中国科学院微生物研究所,中国微生物学会,中国菌物学会
文章信息
- 王安琪, 黄群刚, 康前进, 白林泉. 2021
- Anqi Wang, Qungang Huang, Qianjin Kang, Linquan Bai. 2021
- 安丝菌素聚酮合酶模块2中脱水酶结构域的生化功能
- Biochemical analysis of the dehydratase domain in module 2 involved in ansamitocin biosynthesis
- 微生物学报, 61(3): 607-620
- Acta Microbiologica Sinica, 61(3): 607-620
-
文章历史
- 收稿日期:2020-04-23
- 修回日期:2020-05-20
- 网络出版日期:2020-05-29
2. 上海交通大学代谢与发育国际联合合作实验室, 上海 200240
2. Joint International Research Laboratory of Metabolic & Developmental Sciences, Shanghai Jiao Tong University, Shanghai 200240, China
聚酮类化合物结构丰富多样、生物活性强,是天然药物的重要来源之一[1]。临床上作为药物使用的聚酮类化合物的年销售额已超过了100亿美元[2]。安丝菌素是一种大环内酰胺类化合物,能够阻碍微管蛋白形成,具有良好的抗肿瘤活性,是聚酮类化合物中安莎类化合物的典型代表,具有较大的市场前景。
聚酮化合物由聚酮合酶(Polyketide synthase,PKS)催化形成。已发现的聚酮合酶可以分为Ⅰ型、Ⅱ型和Ⅲ型三大类[3]。其中,Ⅰ型模块化聚酮合酶的线性组装是由若干功能不同的结构域组成,每个结构域在合成过程中仅使用一次,参与聚酮链形成的一步反应[4]。在聚酮化合物的基本生物合成过程中,首先是聚酮链的起始与延伸,由酰基转移酶(Acyl transferase,AT)、酮脂酰-ACP-合成酶(Ketoacyl-ACP synthase,KS)、酰基载体蛋白(Acyl carrier protein,ACP)负责催化[5],然后在聚酮链延伸过程中,聚酮合酶模块中的酮基还原酶(Ketoreductase,KR)将酮基还原成羟基、脱水酶(Dehydratase,DH)负责羟基脱水形成双键、烯键还原酶(Enoylreductase,ER)将双键再次还原形成饱和状态,每个聚酮模块可以不含有或者含有不同的修饰结构域,从而产生多样化的聚酮修饰,最后在硫酯酶(Thioesterase,TE)的催化下进行成熟聚酮链的释放[6]。
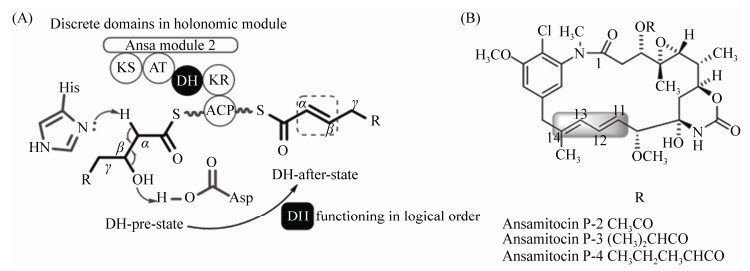
Ⅰ型聚酮类化合物结构多样性的一大来源为聚酮链延伸过程中的不同程度的修饰[7]。在聚酮的碳链修饰中,DH结构域负责完成碳链上β-羟基的脱水,其序列具有保守的“HXXXGXXXXP”基序,保守基序内的组氨酸(H)与基序外的天冬氨酸(D)协同参与,完成α-β脱水形成双键。H负责脱去α质子,质子离去后,D辅助β-羟基的离去并形成α-β双键(图 1-A)[8]。除催化常规α-β脱水外,部分DH结构域还具有其他的特殊功能。如:脱水后催化双键迁移[9],即DH催化已形成的α-β双键迁移至β-γ位[10]、甲基差向异构[11]、双键Z/E异构[12]、环化[13]、烯键γ位脱水[14]等,其中研究最广泛的为双键迁移现象[15]。安莎类化合物中双键迁移的发生普遍与DH结构域相关[16]。
在安丝菌素生物合成过程中共有4个DH结构域催化的脱水反应,其中,Ansa DH2和Ansa DH3结构域对应的C13-C14和C11-C12处发生了脱水反应以及β-γ双键迁移[17] (图 1-B),暗示Ansa DH2与Ansa DH3可能参与催化共轭双键迁移的发生。2009年Kirschning课题组以安丝菌素产生菌Actinosynnema pretiosum ssp. auranticum ATCC31565的AHBA缺失突变株为研究材料,通过底物喂养和转化实验,推测了Asm DH3可能参与了安丝菌素结构中的C11-C12位置双键的迁移[18],但由于缺乏C13-C14双键的三酮化合物的喂养实验,Asm DH2结构域确切的催化特征与功能尚不清楚,仍需要进一步明确。为了对安丝菌素聚酮链延伸模块2中的脱水酶结构域进行更深入的解析,本研究以安丝菌素产生菌Actinosynnema pretiosum subsp. pretiosum ATCC 31280中聚酮合酶模块2中的Ansa DH2为研究对象,利用化学方法经六步线性反应合成了Ansa DH2底物类似物waq-1,并以此为底物对Ansa DH2进行了催化特征分析,结果表明Ansa DH2能够催化α-β脱水,通过体外生化反应完善了Ansa DH2结构域的功能研究,且Ansa DH2底物类似物waq-1的化学全合成也为后续深入研究DH结构域催化的安丝菌素的双键迁移提供了可催化的底物结构,本研究为后续安丝菌素生物合成过程中双键迁移的研究奠定了基础。
1 材料和方法 1.1 材料1.1.1 菌株、质粒及引物: 见表 1。
| Strains/plasmids/primers | Related characters or sequences | Sources or references |
| Strains | ||
| A. pretiosum ATCC 31280 | Ansamitocin producing strain | ATCC |
| Escherichia coli | ||
| DH10B | F– (traΔ36 lacIq proAB lacZΔM15) rpsL (strR) thr leu endA thi-1 lacY galK galT ara tonA tsx dcm dam supE44 Δ(lac-proAB) Δ(mcrC-mrr)102:: Tn10 (tetR) | GIBCO-BRL |
| BL21(DE3) | F– ompT hsdSB(rB–mB–) gal dcm (DE3) | TaKaRa[19] |
| Plasmids | ||
| pET28a | ori-pBR322, Kmr, lac I, His-tag | Novagen |
| pLQ1201 | pET28a-based plasmid for Ansa DH2 expression | This work |
| Primers | Sequences (5′→3′) | |
| Ansa DH2-cF | GGTGATCAGGGAGTGGTCC | |
| Ansa DH2-cR | CAGCCGCGTCGACTCCCAGCG | |
| Ansa DH2-F-Nde I | AAACATATGTGGCTGGACCCC | |
| Ansa DH2-R-Hind Ⅲ | AAAAAGCTTTCAGCGCAGCAGCACCCCC | |
| Ansa DH2-HF-F | CCGTGGCTGGCCGACTTCCGGCTGCTCGAC | |
| Ansa DH2-HF-R | GAAGTCGGCCAGCCACGGGTGGACGCCGGT | |
| Underline: Restriction sites. | ||
1.1.2 主要生化试剂及仪器: 用于化合物萃取与分离的有机试剂如三氯甲烷、乙酸乙酯、甲醇等购自国药集团;用于HPLC及ESI-MS2的乙腈与甲醇购自安捷伦公司;用于核磁鉴定的氘代溶剂购于SIGMA公司;用于化合物合成的原料购自韶远试剂公司;细胞破碎仪购自新芝生物科技有限公司;恒温振荡摇床购自上海知楚有限公司;电子天平购自Sartorius公司;高速离心机购自Thermo Fisher Scientific公司;化合物精确分子量的测定使用Agilent G6540 Q-TOF,核磁共振数据使用Bruker公司的Avance Ⅲ 600MHz核磁共振仪采集。
1.1.3 培养基: 大肠杆菌的培养采用LB及LA培养基[20],放线菌的培养采用TSBY液体培养基(g/L):胰蛋白胨30,酵母提取物10,蔗糖103,pH 7.0–7.2;放线菌活化采用YMG固体培养基(g/L):酵母提取物4,麦芽提取物10,葡萄糖4,琼脂18,pH 7.2–7.4。
1.2 A. pretiosum ATCC 31280总DNA的提取将菌种在YMG固体培养基活化2–3 d,取少量菌体接于新鲜的TSBY培养基30 ℃培养过夜。取200 μL菌液于1.5 mL离心管中,加入500 μL 2 mg/mL溶菌酶,37 ℃水浴30 min破壁处理,加入50 μL 2% SDS。然后,加入250 μL苯酚/氯仿,上下颠倒混匀并用12000 r/min离心5 min,取500 μL上清至新的离心管中,加入50 μL 3 mol/L醋酸钠溶液,混匀后加入500 μL异丙醇沉淀DNA。静置后DNA沉淀析出,捞出絮状的DNA沉淀,用70%乙醇溶液洗涤2次并挥发干乙醇,加入30 μL ddH2O溶解总DNA。
1.3 底物与产物的化学合成以2-甲基苯丙醇为底物,经氧化-酯缩合-羟基保护-酯水解-缩合-羟基脱保护共6步反应得到waq-1,每一步中间产物产物通过1H NMR鉴定,终产物waq-1通过1H NMR与ESI-MS鉴定结构。
化合物2合成:称取化合物1 (1 g, 6.696 mmol)溶于10 mL无水二氯甲烷中,2, 2, 6, 6-四甲基哌啶氮氧化物(10.4 mg,0.067 mmol)溶于5 mL无水二氯甲烷中,缓慢加入反应体系中,随后加入0.5 mL溴化钾(80 mg,0.67 mmol)水溶液,并缓慢加入6%次氯酸钠溶液10 mL,室温搅拌1 h后,经由薄层色谱(TLC)监测反应完毕。分出有机层,水层用60 mL二氯甲烷萃取,合并有机层,依次用1 mol/L的盐酸溶液、饱和硫代硫酸钠与饱和食盐水洗涤有机层。洗涤完毕后,无水硫酸钠干燥1 h,抽滤,旋干滤液。2 g硅胶制砂,30 g硅胶装柱,采用石油醚︰乙酸乙酯=5︰1洗脱得800 mg黄色油状物化合物2,产率为81.04%。
化合物3合成:2 mol/L二异丙基氨基锂-四氢呋喃溶液8.25 mL加入250 mL三颈瓶中,加入10 mL无水四氢呋喃,在氮气保护下干冰丙酮浴冷却至–78 ℃,1.1 g乙酸甲酯溶于10 mL无水四氢呋喃,缓缓滴加入反应体系。滴加完毕后,–78 ℃继续搅拌0.5 h,将化合物2 (2.2 g,16.5 mmol)溶于20 mL无水四氢呋喃中,缓慢滴加至反应液,滴加完毕后控制温度在–78 ℃继续反应2 h,TLC监测反应完毕。冰浴下缓慢滴加饱和氯化铵淬灭反应,真空旋干反应液,加入50 mL水,90 mL乙酸乙酯分3次萃取反应液,合并有机层,并用饱和食盐水洗涤,无水硫酸钠干燥1 h,抽滤,旋干滤液。8 g硅胶制砂,60 g硅胶装柱,采用石油醚︰乙酸乙酯=10︰1洗脱杂质,石油醚︰乙酸乙酯=5︰1洗脱得1.96 g黄色油状化合物3,产率为59.39%。
化合物4合成:称取化合物3 (108 mg, 0.5 mmol)溶于5 mL无水二氯甲烷中,冰浴下加入2, 6-二甲基吡啶(91 μL,0.78 mmol)、叔丁基二甲硅基三氟甲磺酸酯(155 μL,0.68 mmol),继续反应12 h,TLC监测反应完毕。冰浴下缓慢滴加饱和氯化铵淬灭反应,真空旋干反应液,加入10 mL水,30 mL乙酸乙酯分3次萃取,合并有机层,并用饱和食盐水洗涤,无水硫酸钠干燥1 h,抽滤,旋干滤液。0.5 g硅胶制砂,5 g硅胶装柱,采用石油醚︰乙酸乙酯=10︰1洗脱杂质,石油醚︰乙酸乙酯=5︰1洗脱得100 mg黄色油状化合物4,产率为62.11%。
化合物5合成:称取化合物4 (1 g,3 mmol)溶于15 mL无水二氧六环中,加入15%氢氧化钠15 mL,80 ℃加热反应4 h,TLC监测反应完毕。冰浴下缓慢滴加饱和氯化铵淬灭反应,真空旋干反应液,加入30 mL水,60 mL乙酸乙酯分3次萃取,合并有机层,并用饱和食盐水洗涤,无水硫酸钠干燥1 h,抽滤,旋干滤液。2 g硅胶制砂,25 g硅胶装柱,采用石油醚︰乙酸乙酯=5︰1洗脱杂质,石油醚︰乙酸乙酯=2︰1洗脱得950 mg黄色油状化合物5,产率为91.04%。
化合物7合成:称取化合物5 (143 mg,0.46 mmol)溶于5 mL无水N, N-二甲基甲酰胺中,加入N, N'-羰基二咪唑(162 mg,1 mmol),室温搅拌1 h后,加入N-乙酰基半胱胺(122 mg,1.85 mmol),继续室温下搅拌1 h,加入N, N-二甲基吡啶(61 mg,0.46 mmol),室温继续搅拌12 h后TLC监测反应完毕。冰浴下缓慢滴加饱和氯化铵淬灭反应,真空旋干反应液,加入10 mL水,30 mL乙酸乙酯分3次萃取,合并有机层,并用饱和食盐水洗涤,无水硫酸钠干燥1 h,抽滤,旋干滤液。0.5 g硅胶制砂,5 g硅胶装柱,采用石油醚︰乙酸乙酯=2︰1洗脱得180 mg黄色油状化合物7,产率为95.67%。
化合物waq-1合成:称取化合物7 (50 mg,0.12 mmol)溶于1 mL无水乙腈中,加入40%氢氟酸0.5 mL,室温搅拌1 h后,TLC监测反应完毕。冰浴下缓慢滴加pH 7.0的磷酸盐缓冲液5 mL淬灭反应,真空旋干反应液,加入5 mL水,15 mL乙酸乙酯分3次萃取,合并有机层,并用饱和食盐水洗涤,无水硫酸钠干燥1 h,抽滤,旋干滤液。0.5 g硅胶制砂,5 g硅胶装柱,采用石油醚︰乙酸乙酯=1︰1洗脱得25 mg黄色油状物waq-1,产率为68.44%。
1.4 Ansa DH2表达载体的构建、蛋白异源表达与纯化1.4.1 蛋白表达质粒构建: 结合已经报道的红霉素[15]、利福霉素[21]聚酮合酶模块中DH结构域的大小与边界,确定了安丝菌素聚酮合酶Ansa DH2结构域的表达边界。在边界两侧设计外引物Ansa DH2-cF/R,首先以ATCC 31280总DNA为模板,用外引物进行PCR扩增,首轮扩增完毕后,以首轮扩增产物为模板,以携带Nde Ⅰ、Hind Ⅲ酶切位点的内引物Ansa DH2-Nde Ⅰ-F、Ansa DH2- Hind Ⅲ-R进行次轮PCR扩增Ansa DH2结构域,回收0.8 kb的目的条带,经Nde Ⅰ和Hind Ⅲ酶切处理后,胶回收纯化并与相同酶处理的pET 28a载体相连接,构建Ansa DH2表达质粒pLQ1201,将其导入E. coli BL21(DE3),获得蛋白表达菌株。
1.4.2 蛋白表达: 将蛋白表达菌株接于含有50 mg/L卡那霉素的LB培养基中,37 ℃培养12–16 h,而后以1%的接种量转接到含有50 mg/L卡那霉素的LB培养基中,37 ℃培养至OD600 0.6–0.8,然后加入终浓度为0.4 mmol/L的IPTG,16 ℃诱导16–20 h。表达完毕后,5000 r/min离心10 min收集菌体,使用50 mmol/L Tris-HCl、500 mmol/L NaCl配置的Binding Buffer (pH 8.0)洗涤菌体,–80 ℃保存备用。
1.4.3 蛋白纯化: 将菌体重悬在4 ℃预冷的50 mmol/L Tris-HCl、500 mmol/L NaCl的Binding Buffer (pH 8.0)中,超声破碎。4 ℃、12000 r/min离心30 min分离上清和细胞沉淀。取上清进行镍亲和层析,分别以Binding Buffer、Binding Buffer添加15 mmol/L咪唑和50 mmol/L咪唑洗去杂蛋白,再用Binding Buffer添加250 mmol/L咪唑洗脱目标蛋白。目标蛋白经超滤脱盐并浓缩后,利用SDS-PAGE检测蛋白纯化情况,并用于体外生化反应。
1.5 Ansa DH2结构域的定点突变以质粒pLQ1201为模板,用携带突变位点的上下游引物Ansa DH2-HF-F、Ansa DH2-HF-R进行PCR扩增,产物用Dpn I酶解去除模板质粒。经胶回收纯化后,用DNA连接酶solution I于16 ℃连接1 h,转入E. coli DH 10B感受态细胞。经筛选和测序验证后,提取突变质粒,导入E. coli BL21(DE3),完成蛋白定点突变表达菌株的构建。将定点突变表达菌株进行蛋白诱导表达与纯化,测试定点突变蛋白的体外生化反应活性。
1.6 酶促反应体系的建立与产物分离1.6.1 反应体系Buffer筛选: 在10 μL反应体系中加入5 mmol/L底物和终浓度为2 mg/mL的酶,分别使用HEPES及Tris-HCl缓冲液(pH 7.5),30 ℃恒温孵育24 h。加入20 μL甲醇终止反应,利用HPLC检测反应物与产物含量,确定适宜的反应缓冲液。
1.6.2 时间曲线绘制: 在70 μL反应体系中加入5 mmol/L底物和终浓度为2 mg/mL的酶,使用Tris-HCl缓冲液(pH 8.5),30 ℃恒温孵育1、2、4、10、16、36 h。分别取10 μL反应液,加入20 μL甲醇终止反应,利用HPLC鉴定产物与反应物含量,绘制时间曲线,确定反应时间。
1.6.3 产物的分离与鉴定: 在反应液中加入2倍体积乙酸乙酯萃取3次,将萃取液合并、旋干并溶于5 μL乙酸乙酯。以254 nm荧光为指示,薄层色谱法在硅胶板上分离反应物与产物。将产物点回收,溶于丙酮,蒸干溶剂后溶于乙腈,利用ESI-MS2鉴定结构。
1.7 LC-MS检测用于检测的色谱柱为Agilent Eclipse plus C18 (4.6 mm×150 mm,直径5 μm)。洗脱流动相为:MeCN-H2O (0.1% HCOOH)。洗脱程序为:0–5 min为90%的A相(V/V)平衡色谱柱;5–25 min为90%–10%的A相(V/V)梯度洗脱;25–28 min为10%的A相(V/V)洗脱;28–30 min为90%的A相(V/V)。检测采用阳离子模式,ESI源进行分子量鉴定。
2 结果和分析 2.1 Ansa DH2的生物信息学分析经氨基酸序列比对分析,安丝菌素聚酮合酶模块1、2、3和6中的DH结构域与已经解析晶体结构的红霉素生物合成聚酮合酶模块4 (Ery DH4)及利福霉素生物合成聚酮合酶模块10 (Rif DH10)中的DH结构域同源性较高(图 2-A)。以Ansa DH2为例,在“HXXXGXXXXP”保守基序中的48位H残基完成α-质子离去,与211位的D残基共同完成脱水。从氨基酸序列上分析,安丝菌素聚酮合酶模块1、2、3和6中的脱水酶结构域都含有负责质子离去的H和羟基离去的D (Ansa DH3对应位置为性质类似的E),均具有脱水活性。

|
| 图 2 Ansa DH生物信息学分析 Figure 2 Bioinformatics analysis of Ansa DHs with their homologs. A: Homologous evolution of Ansa DH amino acids with conserved residues highlighted. All DH domains show high similarity. Based on sequence analysis, four Ansa DHs should have the ability to catalyze dehydration; B: Phylogenetic tree of DH domains shows that Ansa DH2 and Ansa DH3 (highlighted with black dots) possess much higher homology with DHs (highlighted with gray dots), which might be responsible for the olefin shift. |
将Ansa DH序列在NCBI进行BLAST寻找同源性较高的序列,使用MEGA X[22]以最大似然原则及JTT矩阵模型[23]对Ansa DH2和Ansa DH3进行系统进化分析,构建系统进化树[24],依据同源性进行无监督聚类发现,Ansa DH2与Ansa DH3结构域从系统进化角度较为接近,同源性为36%。此外,结合催化双键迁移的Amb DH4、Cha DH4和Vic DH5可以发现[11, 16],Ansa DH2及Ansa DH3与催化双键迁移的Cha DH4和Vic DH5同源性均超过30% (图 2-B)。与催化双键迁移的DH结构域的较高同源性暗示着Ansa DH2及Ansa DH3可能与安丝菌素C13-C14、C11-C12位置的双键迁移相关。为了证明Ansa DH2的脱水作用,确定其是否能够催化安丝菌素C13-C14双键迁移,需要合成其底物进行体外生化反应分析。
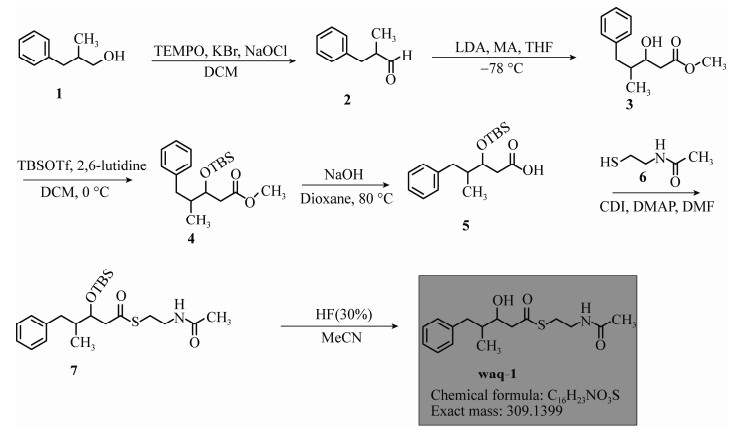
2.2 Ansa DH2结构域的底物类似物的化学全合成根据文献报道,体外酶促反应多以SNAC (N-乙酰基半胱胺)衍生物模拟体内ACP活化的底物[25]。为了便于研究Ansa DH2结构域的功能,我们以化合物1为原料,利用1.3中的方法,经过六步反应合成了Ansa DH2底物类似物waq-1,作为Ansa DH2生化功能研究的底物(图 3)。对每一步中间产物和终产物分别进行了1H NMR的结构鉴定,waq-1的终产率为17.81%。
|
| 图 3 waq-1的化学合成路线 Figure 3 Chemical synthesis route of waq-1. |
中间产物2的结构鉴定如下:1H NMR (400 MHz, DMSO-d6) δ 9.67 (s, 1H), 7.29 (t, J= 7.5 Hz, 2H), 7.24–7.14 (m, 3H), 3.03 (dd, J=13.6, 6.0 Hz, 1H), 2.72 (dd, J=14.0, 7.0 Hz, 1H), 2.58 (dd, J=13.5, 8.0 Hz, 1H), 0.95 (d, J=7.0 Hz, 3H)。
中间产物3的结构鉴定如下:1H NMR (400 MHz, DMSO-d6) δ 7.27 (t, J=7.5 Hz, 2H), 7.17 (t, J=6.7 Hz, 3H), 4.82 (dd, J=29.0, 5.7 Hz, 1H), 3.80 (m, 1H), 3.59 (d, J=8.7 Hz, 3H), 2.85–2.71 (m, 1H), 2.59–2.20 (m, 3H), 0.74 (dd, J=9.5, 6.9 Hz, 3H)。
中间产物4的结构鉴定如下:1H NMR (400 MHz, CDCl3-d) δ 7.35–7.27 (m, 2H), 7.25–7.14 (m, 3H), 4.20 (m, 1H), 3.71 (d, J=0.6 Hz, 3H), 2.88 (ddd, J=18.7, 13.3, 4.5 Hz, 1H), 2.50 (dd, J=6.4, 3.3 Hz, 2H), 2.27 (ddd, J=24.0, 13.3, 10.2 Hz, 1H), 2.02–1.86 (m, 1H), 0.94 (t, J=11.8 Hz, 9H), 0.89–0.79 (m, 3H), 0.18–0.02 (m, 6H)。
中间产物5的结构鉴定如下:1H NMR (400 MHz, DMSO-d6) δ 7.35–7.12 (m, 5H), 4.11 (m, 1H), 2.94–2.63 (m, 1H), 2.52–2.37 (m, 2H), 2.37–2.21 (m, 2H), 0.94–0.84 (m, 9H), 0.83–0.72 (m, 3H), 0.13– –0.05 (m, 6H)。
中间产物7的结构鉴定如下:1H NMR (400 MHz, CDCl3-d) δ 7.28 (ddd, J=7.5, 5.9, 2.8 Hz, 2H), 7.23–7.16 (m, 1H), 7.16–7.10 (m, 2H), 5.92 (s, 1H), 4.25–4.14 (m, 1H), 4.14–4.09 (m, 1H), 3.52– 3.35 (m, 2H), 3.13–2.91 (m, 3H), 2.86–2.62 (m, 3H), 2.25 (ddd, J=23.9, 13.3, 10.0 Hz, 1H), 2.05– 1.96 (m, 3H), 0.94–0.90 (m, 3H), 0.88–0.76 (m, 9H), 0.12– –0.05 (m, 6H)。
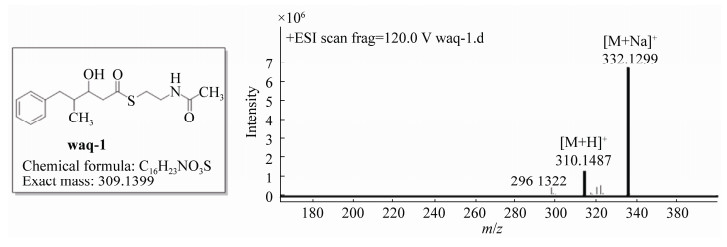
waq-1的结构鉴定如下:1H NMR (400 MHz, CDCl3-d) δ 7.28 (t, J=7.2 Hz, 2H), 7.18 (dd, J= 13.4, 7.4 Hz, 3H), 6.05 (s, 1H), 4.10–3.88 (m, 1H), 3.44 (dd, J=15.3, 10.5 Hz, 2H), 3.13–2.97 (m, 2H), 2.94–2.82 (m, 2H), 2.82 – 2.64 (m, 2H), 2.41 (ddd, J=22.5, 13.4, 9.0 Hz, 1H), 1.97 (d, J=2.4 Hz, 3H), 0.87 (dd, J=16.3, 6.8 Hz, 3H) (图 4)。
|
| 图 4 waq-1的ESI-MS分析 Figure 4 ESI-MS profile of waq-1. |
2.3 Ansa DH2结构域的酶促反应体系优化
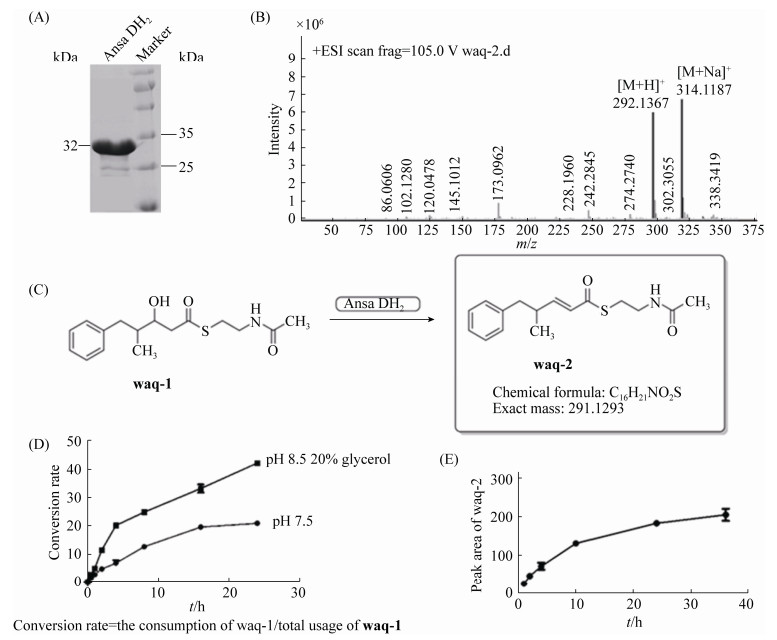
按照1.4所示方法构建蛋白表达菌株,进行蛋白的诱导表达,经镍柱亲和层析法可纯化获得Ansa DH2蛋白(图 5-A)。按照1.6所述方法,以waq-1为底物对不同反应缓冲液进行选择。最后,使用Tris-HCl作为反应缓冲液,30 ℃反应24 h时,转化率可以达到19.47%,且可有效降低副产物的含量。
|
| 图 5 Ansa DH2体外实验结果 Figure 5 In vitro test of Ansa DH2. A: SDS-PAGE analysis of Ansa DH2. B: LC-ESI-MS analysis of the product. C: Putative function of Ansa DH2. D: Conversion rate of waq-1 using different buffers. With 20% glycerol added in Tris-HCl (pH 8.5), the conversion rate of waq-1 has increased to 41%. E: Ansa DH2 time course in Tris-HCl (pH 8.5) adding 20% glycerol. The peak area of waq-2 increased slowly after 24 h. |
按照1.6的方法使用TLC对产物进行分离,采用LC-ESI-MS测得产物分子量与waq-1脱水化合物waq-2一致(图 5-B),推测Ansa DH2结构域可以催化底物类似物waq-1完成脱水(图 5-C)。反应过程中观察到蛋白迅速沉淀并失活,反应效率极低。多元醇常用来提高蛋白的溶解性,甘油作为一种常见饱和多元醇常用于稳定蛋白[26]。有研究表明甘油可提高蛋白热稳定性[27]与溶解度[28]。通过在反应体系中添加终浓度为20%的甘油,结合Ansa DH2等电点(pI=6.04)将反应液pH优化至8.5后,提高了蛋白溶解性,24 h的催化转化率提高到41% (图 5-D)。适度延长反应时间至36 h,经HPLC检测waq-2的产量略有提升,产率由41%提高至45%。结合转化率兼顾反应效率,最终确定反应时间为36 h (图 5-E)。
经过反应缓冲液的筛选、甘油的添加、pH及反应时间的优化,将36 h的反应效率提高至45%左右,确定最适反应条件为5 mmol/L底物、终浓度为2 mg/mL的酶、Tris-HCl缓冲液(pH 8.5)、终浓度为20%的甘油,30 ℃孵育36 h。
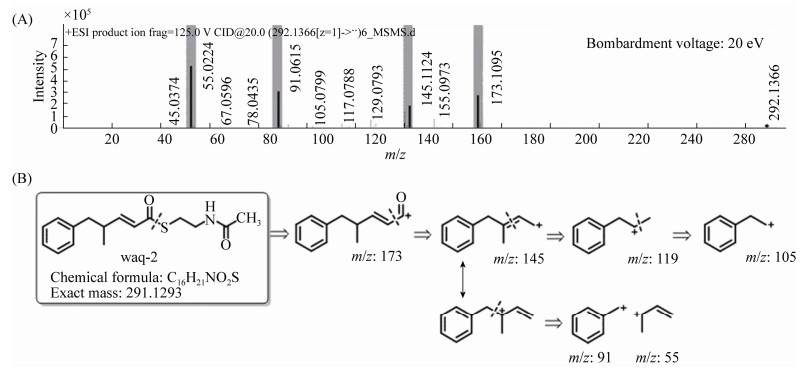
2.4 Ansa DH2结构域催化了α-β脱水按照1.6所述方法将产物纯化并进行二级质谱分析,采用分子断裂碎片来确定产物结构。通过ESI-MS确定产物精确分子量后,以不同电压轰击产物分子,得到不同轰击电压下产物二级质谱断裂碎片,其中以20 eV轰击时,断裂碎片为特征(图 6-A)。在20 eV轰击时,产物分子硫酯键发生σ断裂,二级质谱可以发现产物分子去除SNAC的m/z 173碎片峰。此外,还可以得到m/z 173碎片脱去羰基的m/z 145碎片峰、m/z 145碎片发生烯丙基位断裂的m/z 91碎片峰和m/z 55碎片峰。通过其断裂模式可初步判断Ansa DH2催化底物类似物的α-β脱水(图 6-B)。
|
| 图 6 产物waq-2的结构鉴定 Figure 6 The elucidation of the structure of waq-2. A: The profiles of MS2 at bombardment voltage 20 eV with characteristic fragmentations highlighted; B: Putative fragmentations of waq-2. |
在以waq-1为底物的反应条件下,通过MS2断裂碎片分析可知,Ansa DH2可催化完成α-β脱水,这说明Ansa DH2结构域拥有α-β脱水功能,这为后续研究安丝菌素聚酮延伸过程中的双键迁移现象奠定了实验基础。
2.5 Ansa DH2结构域催化脱水的关键氨基酸残基的确定为了对DH结构域的脱水机制进行初步解析,采用定点突变的策略证明Ansa DH2结构域中的保守位点H是活性必需氨基酸。H的拔质子作用来源于碱性侧链基团,参考氨基酸性质及侧链基团大小,将Ansa DH2结构域保守位点即第48位的组氨酸突变成了残基大小较为接近的中性氨基酸苯丙氨酸(F)。依据1.5的方法构建定点突变蛋白表达菌株,经诱导表达与镍柱亲和层析,纯化获得Ansa DH2 (H48F)蛋白(图 7-A)。在Ansa DH2的最适反应条件下,Ansa DH2 (H48F)突变蛋白无法催化脱水反应,而阳性对照经TLC检测可获得产物(图 7-B)。因此,Ansa DH2结构域具有催化脱水的活性,48位的H为脱水活性的关键氨基酸。

|
| 图 7 Ansa DH2 (H48F)突变蛋白的体外实验结果 Figure 7 In vitro analysis of Ansa DH2 (H48F). A: SDS-PAGE analysis of Ansa DH2 (H48F). B: TLC analysis. Ansa DH2 (H48F): TLC analysis of incubation of Ansa DH2 (H48F); Ansa DH2 (P): TLC analysis of incubation of purified Ansa DH2; Ansa DH2 (S): TLC analysis of incubation of unpurified protein supernatant; substrate: TLC analysis of waq-1. |
3 讨论
聚酮类化合物生物合成过程中的不同链长、PKS延伸过程中的修饰以及复杂的PKS合成后修饰,产生了多种多样的聚酮类化合物[29]。结构多样性导致生物活性多样性[30],这使其成为药物开发的重要来源[31]。安丝菌素是一种大环内酰胺类化合物,它能够与微管蛋白β亚基结合,阻碍微管蛋白的组装,具有显著的抗肿瘤活性,还能够抑制真菌、酵母等真核生物的生长[32],有重要的临床应用价值。
通过系统进化分析发现,安丝菌素聚酮合酶DH结构域中的Ansa DH2及Ansa DH3结构域与催化双键迁移的DH结构域同源性更高。通过优化Ansa DH2反应缓冲液与pH,将36 h反应效率由初始的19.47%提高至45%;通过ESI-MS2鉴定产物结构,证实了Ansa DH2可以催化α-β脱水;对Ansa DH2第48位H进行了定点突变,证明了H为脱水活性的必需氨基酸。由于waq-1与Ansa DH2真实底物存在区别以及SNAC衍生与ACP结构域上载的差异,因此Ansa DH2体内能否催化双键迁移仍需要进一步验证。后续还需要对其天然底物进行合成,并经由ACP上载进行体外生化反应进行确认。
不同于已被充分解析的脂肪酸合成过程中的双键迁移现象[33],包括安丝菌素在内的具有共轭双键迁移的聚酮类化合物中,其双键迁移机制尚未研究透彻。共轭双键的迁移很可能是由于DH结构域的底物口袋以及催化位点附近的氨基酸的作用。双键迁移所导致的化合物结构多样性为发现更多具有优良药理活性的衍生物提供了可能性;此外,利用DH结构域催化双键迁移的功能可以将双键迁移至易于衍生的位置(如部分聚酮化合物中的末端烯键等),极大地方便后续的化学修饰。基于此还可以对化合物进行理性设计与定向改造,有研究表明对DH-KR结构域的PKS模块改造可以提高低毒性匹马霉素衍生物的相对含量[34]。在确定负责催化安丝菌素双键迁移的脱水酶结构域后,可以对其进行晶体结构的解析与计算,在晶体结构的指导下确定共轭双键迁移与脱水酶反应中心关键氨基酸的关联性,并以此为依据,尝试对聚酮合酶进行设计与改造,以期得到更多的结构新颖、生物活性强的聚酮化合物。
| [1] | Tan GY, Liu TG. Rational synthetic pathway refactoring of natural products biosynthesis in actinobacteria. Metabolic Engineering, 2017, 39: 228-236. DOI:10.1016/j.ymben.2016.12.006 |
| [2] |
Rong H, Huang HQ, Bao SX. Research progresses on biosynthesizing polyketides in heterologous hosts. Natural Product Research and Development, 2007, 19(6): 1097-1100, 1078.
(in Chinese) 荣辉, 黄惠琴, 鲍时翔. 异源生物合成聚酮化合物的研究进展. 天然产物研究与开发, 2007, 19(6): 1097-1100, 1078. |
| [3] | Shen B. Polyketide biosynthesis beyond the type Ⅰ, Ⅱ and Ⅲ polyketide synthase paradigms. Current Opinion in Chemical Biology, 2003, 7(2): 285-295. DOI:10.1016/S1367-5931(03)00020-6 |
| [4] | Keatinge-Clay AT. The structures of type Ⅰ polyketide synthases. Natural Product Reports, 2012, 29(10): 1050-1073. DOI:10.1039/c2np20019h |
| [5] | Hopwood DA. Genetic contributions to understanding polyketide Synthases. Chemical Reviews, 1997, 97(7): 2465-2498. DOI:10.1021/cr960034i |
| [6] | Holzbaur IE, Harris RC, Bycroft M, Cortes J, Bisang C, Staunton J, Rudd BAM, Leadlay PF. Molecular basis of Celmer's rules: the role of two ketoreductase domains in the control of chirality by the erythromycin modular polyketide synthase. Chemistry & Biology, 1999, 6(4): 189-195. |
| [7] | Fischbach MA, Walsh CT. Assembly-line enzymology for polyketide and nonribosomal peptide antibiotics: Logic, machinery, and mechanisms. Chemical Reviews, 2006, 106(8): 3468-3496. DOI:10.1021/cr0503097 |
| [8] | Weissman KJ. Uncovering the structures of modular polyketide synthases. Natural Product Reports, 2015, 32(3): 436-453. DOI:10.1039/C4NP00098F |
| [9] | Moldenhauer J, Gotz DC, Albert CR, Bischof SK, Schneider K, Sussmuth RD, Engeser M, Gross H, Bringmann G, Piel J. The final steps of bacillaene biosynthesis in Bacillus amyloliquefaciens FZB42:direct evidence for β, γ dehydration by a trans-acyltransferase polyketide synthase. Angewandte Chemie-International Edition, 2010, 49(8): 1465-1467. DOI:10.1002/anie.200905468 |
| [10] | Kusebauch B, Busch B, Scherlach K, Roth M, Hertweck C. Functionally distinct modules operate two consecutive α, β→β, γ double-bond shifts in the rhizoxin polyketide assembly line. Angewandte Chemie-International Edition, 2010, 49(8): 1460-1464. DOI:10.1002/anie.200905467 |
| [11] | Berkhan G, Merten C, Holec C, Hahn F. The Interplay between a multifunctional dehydratase domain and a C-methyltransferase effects olefin shift in ambruticin biosynthesis. Angewandte Chemie-International Edition, 2016, 55(43): 13589-13592. DOI:10.1002/anie.201607827 |
| [12] | Dodge GJ, Ronnow D, Taylor RE, Smith JL. Molecular basis for olefin rearrangement in the gephyronic acid polyketide synthase. ACS Chemical Biology, 2018, 13(9): 2699-2707. DOI:10.1021/acschembio.8b00645 |
| [13] | Sung KH, Berkhan G, Hollmann T, Wagner L, Blankenfeldt W, Hahn F. Insights into the dual activity of a bifunctional dehydratase-cyclase domain. Angewandte Chemie- International Edition, 2018, 57(1): 343-347. DOI:10.1002/anie.201707774 |
| [14] | Fiers WD, Dodge GJ, Sherman DH, Smith JL, Aldrich CC. Vinylogous dehydration by a polyketide dehydratase domain in curacin biosynthesis. Journal of the American Chemical Society, 2016, 138(49): 16024-16036. DOI:10.1021/jacs.6b09748 |
| [15] | Keatinge-Clay A. Crystal structure of the erythromycin polyketide synthase dehydratase. Journal of Molecular Biology, 2008, 384(4): 941-953. DOI:10.1016/j.jmb.2008.09.084 |
| [16] | Keatinge-Clay AT. The uncommon enzymology of cis-acyltransferase assembly lines. Chemical Reviews, 2017, 117(8): 5334-5366. DOI:10.1021/acs.chemrev.6b00683 |
| [17] | Kang QJ, Shen YM, Bai LQ. Biosynthesis of 3, 5-AHBA-derived natural products. Natural Product Reports, 2012, 29(2): 243-263. DOI:10.1039/C2NP00019A |
| [18] | Taft F, Brünjes M, Knobloch T, Floss HG, Kirschning A. Timing of the Δ10, 12-Δ11, 13 double bond migration during ansamitocin biosynthesis in Actinosynnema pretiosum. Journal of the American Chemical Society, 2009, 131(11): 3812-3813. DOI:10.1021/ja8088923 |
| [19] | Moffatt BA, Studier FW. T7 lysozyme inhibits transcription by T7 RNA polymerase. Cell, 1987, 49(2): 221-227. DOI:10.1016/0092-8674(87)90563-0 |
| [20] | Rebets Y, Brotz E, Manderscheid N, Tokovenko B, Myronovskyi M, Metz P, Petzke L, Luzhetskyy A. Insights into the pamamycin biosynthesis. Angewandte Chemie-International Edition, 2015, 54(7): 2280-2284. DOI:10.1002/anie.201408901 |
| [21] | Gay D, You YO, Keatinge-Clay A, Cane DE. Structure and stereospecificity of the dehydratase domain from the terminal module of the rifamycin polyketide synthase. Biochemistry, 2013, 52(49): 8916-8928. DOI:10.1021/bi400988t |
| [22] | Kumar S, Stecher G, Li M, Knyaz C, Tamura K. MEGA X: molecular evolutionary genetics analysis across computing platforms. Molecular Biology and Evolution, 2018, 35(6): 1547-1549. DOI:10.1093/molbev/msy096 |
| [23] | Jones DT, Taylor WR, Thornton JM. The rapid generation of mutation data matrices from protein sequences. Computer Applications in the Biosciences, 1992, 8(3): 275-282. |
| [24] | Eickmeyer K, Huggins P, Pachter L, Yoshida R. On the optimality of the neighbor-joining algorithm. Algorithms for Molecular Biology, 2008, 3: 5. DOI:10.1186/1748-7188-3-5 |
| [25] | Li Y, Dodge GJ, Fiers WD, Fecik RA, Smith JL, Aldrich CC. Functional characterization of a dehydratase domain from the pikromycin polyketide synthase. Journal of the American Chemical Society, 2015, 137(22): 7003-7006. DOI:10.1021/jacs.5b02325 |
| [26] | Wang W. Protein aggregation and its inhibition in biopharmaceutics. International Journal of Pharmaceutics, 2005, 289(1/2): 1-30. |
| [27] | Baier SK, Decker EA, McClements DJ. Impact of glycerol on thermostability and heat-induced gelation of bovine serum albumin. Food Hydrocolloids, 2004, 18(1): 91-100. DOI:10.1016/S0268-005X(03)00046-8 |
| [28] | Kamerzell TJ, Esfandiary R, Joshi SB, Middaugh CR, Volkin DB. Protein-excipient interactions: mechanisms and biophysical characterization applied to protein formulation development. Advanced Drug Delivery Reviews, 2011, 63(13): 1118-1159. DOI:10.1016/j.addr.2011.07.006 |
| [29] | McDaniel R, Ebert-Khosla S, Hopwood DA, Khosla C. Engineered biosynthesis of novel polyketides: manipulation and analysis of an aromatic polyketide synthase with unproven catalytic specificities. Journal of the American Chemical Society, 1993, 115(25): 11671-11675. DOI:10.1021/ja00078a002 |
| [30] | Hopwood DA, Sherman DH. Molecular genetics of polyketides and its comparison to fatty acid biosynthesis. Annual Review of Genetics, 1990, 24: 37-62. DOI:10.1146/annurev.ge.24.120190.000345 |
| [31] | Newman DJ, Cragg GM. Natural products as sources of new drugs from 1981 to 2014. Journal of Natural Products, 2016, 79(3): 629-661. DOI:10.1021/acs.jnatprod.5b01055 |
| [32] | Tanida S, Hasegawa T, Hatano K, Higashide E, Yoneda M. Ansamitocins, maytansinoid antitumor antibiotics producing organism, fermentation, and antimicrobial activities. The Journal of Antibiotics, 1980, 33(2): 192-198. DOI:10.7164/antibiotics.33.192 |
| [33] | Liavonchanka A, Rudolph MG, Tittmann K, Hamberg M, Feussner I. On the mechanism of a polyunsaturated fatty acid double bond isomerase from Propionibacterium acnes. Journal of Biological Chemistry, 2009, 284(12): 8005-8012. DOI:10.1074/jbc.M809060200 |
| [34] | Qi Z, Zhou YC, Kang QJ, Jiang CY, Zheng JT, Bai LQ. Directed accumulation of less toxic pimaricin derivatives by improving the efficiency of a polyketide synthase dehydratase domain. Applied Microbiology and Biotechnology, 2017, 101(6): 2427-2436. DOI:10.1007/s00253-016-8074-7 |
 2021, Vol. 61
2021, Vol. 61