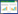中国科学院微生物研究所,中国微生物学会
文章信息
- 叶乐, 甄向凯, 欧阳松应. 2023
- YE Le, ZHEN Xiangkai, OUYANG Songying.
- 原核生物Ⅶ型毒素-抗毒素系统研究进展
- Progress of type Ⅶ toxin-antitoxin system in prokaryotes
- 微生物学报, 63(3): 993-1007
- Acta Microbiologica Sinica, 63(3): 993-1007
-
文章历史
- 收稿日期:2022-08-04
- 网络出版日期:2022-10-13
毒素-抗毒素(toxin-antitoxin, TA)系统在细菌染色体和质粒上普遍存在,通常位于同一操纵子下,由分别编码毒素的基因和编码抗毒素的基因组成。大多数毒素为蛋白,在细菌细胞中较为稳定,抗毒素为蛋白或非编码RNA,且容易被降解[1]。在细菌正常生长过程中,毒素的毒性会被抗毒素中和。当细菌遭遇不利环境时,例如营养缺乏、DNA损伤、抗生素作用、噬菌体入侵等,抗毒素则会被降解,毒素被释放,通过干扰细菌必需的生命活动,如膜的完整性、细胞壁合成、蛋白质的翻译、DNA复制和细胞骨架的形成等,进而改变细菌自身的代谢以应对不利的环境。当应激条件消失后,抗毒素重新被合成,毒素的毒性再次被抗毒素中和,细菌恢复生长[2]。TA系统的毒素不同于细菌在生长过程中产生的各类毒素—包括由细胞分泌到细胞外的外毒素(exotoxin)和由于菌体裂解后而释放出的细菌内毒素(endotoxin)。TA系统的抗毒素也不同于免疫治疗中通过这些毒素免疫高等动物,得到具有中和作用的特异性抗体或血清(抗毒素)[3]。到目前为止,已经发现的TA系统可以分为Ⅰ‒Ⅷ型,其中Ⅱ型TA的研究最为广泛[4]。最新发现的Ⅶ型TA与Ⅱ型TA较为相似,两类TA的毒素和抗毒素都是蛋白质,但两者作用机制完全不同。Ⅱ型TA主要通过抗毒素与毒素的直接结合,来中和毒素的毒性,而Ⅶ型TA则是依赖抗毒素对毒素进行翻译后修饰,来消除毒素的毒性[5]。与Ⅱ型TA一样,Ⅶ型TA大量存在于微生物中,然而关于它们的研究相对较少,对Ⅶ型TA的研究有利于进一步了解TA系统与致病菌毒力之间的关系。
1 TA系统分类根据毒素抗毒素的性质以及中和毒素的方式,TA系统被分为Ⅰ‒Ⅷ型。在Ⅰ型到Ⅶ型TA中,毒素是蛋白质,而在Ⅷ型TA中,毒素与抗毒素都是非编码小RNA[6],在Ⅰ型、Ⅲ型和Ⅷ型TA中,抗毒素是小的非编码RNA,而在Ⅱ型、Ⅳ型、Ⅴ型、Ⅵ型和Ⅶ型TA中,抗毒素是小蛋白质[7],如图 1所示。
1.1 Ⅰ型TA
在Ⅰ型TA中,抗毒素是RNA,能够抑制毒素mRNA的翻译[9]。最先发现的Ⅰ型TA是hok-sok系统[10]。Ⅰ型TA中的毒素大多是针对细菌膜完整性的小疏水肽,能破坏细胞膜,抑制细胞分裂[9]。在大肠杆菌的hok-sok系统中,抗毒素通过抑制先导肽的翻译发挥作用。抗毒素Sok碱基与mok的核糖体结合位点结合,mok是一种重要的先导肽,因此间接阻止了Hok毒素的翻译。而在大肠杆菌中的tisB-istR系统中,在毒素TisB的翻译起始位点上游存在100个核苷酸,这段核苷酸序列能够与核糖体结合,是毒素TisB翻译必需的,抗毒素IstR能够与这段序列结合,从而抑制毒素蛋白的翻译[11],此外Ⅰ型TA还有symE-symR系统、ldrD-rdlD系统等,Ⅰ型TA通常与细菌抵抗噬菌体相关[12]。除了抑制翻译外,毒素抗毒素形成的RNA双链也是细胞RNA酶的靶标,抗毒素的结合最终导致毒素的mRNA发生降解[13]。
1.2 Ⅱ型TAⅡ型TA是所有TA系统中研究得最多的一类,Ⅱ型TA中毒素与抗毒素都是蛋白,抗毒素能够与毒素形成稳定的复合物,从而中和毒素[14]。与Ⅰ型TA不同,这两个基因通常在同一启动子下,抗毒素一般位于毒素基因的上游[4]。在营养缺乏、高温、氧化应激、噬菌体感染或抗生素压力等应激条件下,细胞内的抗毒素被蛋白酶降解,毒素从抗毒素毒素复合物中被释放[15],Lon、ClpAP和ClpXP属于ATP依赖性蛋白酶,在应激条件下能参与抗毒素的降解[16]。Ⅱ型TA根据毒素的功能和结构特征分为relBE、mazEF、vapBC、ccdAB、parDE、higAB、hipBA和Phd-Doc等家族。抗毒素和毒素转录水平上的差异也能够调节TA系统,这种机制叫作“条件协同性”[17]。在定量分析大肠杆菌relBE的TA系统后发现,不同化学计量比的毒素和抗毒素会形成异聚体,而作用最强的转录阻遏物是具有这2种蛋白质中间比例的复合物。当抗毒素RelB超过毒素RelE时,抗毒素形成二聚体RelB2,可抑制relBE启动子。并且2:1的RelB2:RelE复合物对relBE启动子表现出最强的转录抑制作用。然而2:2的RelB2:RelE2复合物无法与启动子结合,此时转录仍处于激活状态[17]。目前为止,发现的所有的TA系统都具有条件协同性,这是TA系统较为普遍的特征[17]。不同的Ⅱ型TA具有不同的作用,例如铜绿假单胞菌中higAB系统会影响其他毒力因子表达[18],包括yefM-yoeB在内的一些其他Ⅱ型TA系统有助于宿主细胞内细菌的存活[19],mqsRA系统参与了生物被膜的形成[20],毒素蛋白HipA有助于持留菌的形成[21]。
1.3 Ⅲ型TAⅢ型TA的抗毒素是RNA,能够与毒素蛋白直接结合,目前已知的Ⅲ型TA主要有3个家族,分别是toxIN、tenpIN和cptIN,toxIN系统是最早发现的Ⅲ型TA[22]。ToxN毒素具有核糖核酸内切酶活性,可通过与抗毒素(ToxI)相互作用形成大分子复合物[23]。三聚体毒素抗毒素复合物是通过3个ToxN蛋白和3个ToxI单体相互作用形成的,从而抑制ToxN毒素[23]。在toxN基因之前有一系列的直接重复和短的反向重复序列,抗毒素重复序列被认为是Ⅲ型TA的关键特征。toxIN系统的主要功能是通过促进细菌的流产性感染,抵抗噬菌体感染[24]。
1.4 Ⅳ型TAⅣ型TA系统的毒素和抗毒素都是蛋白质,但是抗毒素不是直接通过相互作用抑制毒素毒性,而是通过与毒素竞争性结合毒素的底物,从而抑制毒素蛋白的毒性[25]。在大肠杆菌中最早发现的Ⅳ型TA是cbeA-cbtA系统[25]。毒素蛋白CbtA能够与细胞骨架蛋白MreB和FtsZ结合,阻止细胞骨架蛋白聚合,从而改变细胞形态,最终导致细胞溶解。抗毒素蛋白CbeA能够与MreB和FtsZ蛋白结合,稳定细胞骨架,消除毒素CbtA的毒性[26]。
1.5 Ⅴ型TAV型TA的抗毒素是蛋白质,但不直接与毒素结合,而是通过降解毒素的mRNA,抑制毒素的表达[27]。目前唯一的Ⅴ型TA是ghoST系统,毒素蛋白GhoT能够损伤细胞膜,导致细胞死亡,抗毒素GhoS具有核糖核酸内切酶活性,能够降解毒素蛋白GhoT的mRNA[27]。
1.6 Ⅵ型TAⅥ型TA最早是在革兰氏阴性菌新月柄杆菌(Caulobacter crescentus)中发现,毒素与抗毒素都是蛋白质[28]。最先鉴定的Ⅵ型TA是socA-socB系统,socAB系统中毒素蛋白SocB与抗毒素蛋白SocA能够直接结合,但不能使毒素蛋白失活,而是在抗毒素在结合毒素蛋白之后,通过结合蛋白酶体,降解毒素蛋白[28]。
1.7 Ⅶ型TAⅦ型TA的毒素和抗毒素都是蛋白质,已经鉴定的Ⅶ型TA分为3种:HepT/MntA系统、Rv1045/Rv1044系统和Hha-TomB系统[5]。Ⅶ型TA作为最近发现的新型TA,其机制与Ⅱ型TA明显不同,Ⅱ型TA中的抗毒素通常是与DNA结合的转录因子,Ⅶ型TA中抗毒素则是一类酶,并且Ⅶ型TA中毒素毒性的中和不是基于与抗毒素的直接相互作用,而是依赖于抗毒素对毒素活性位点进行翻译后修饰[29]。
1.8 Ⅷ型TAⅧ型TA系统的毒素与抗毒素都是非编码的小RNA,目前鉴定的Ⅷ型TA主要为CreT/CreA系统,该系统位于CRISPR-Cas系统cas6和cas8基因间,与CRISPR-Cas系统发生偶联,毒素级联抑制毒素(cascade-repressed toxin, CreT)受cascade的调控,其5′端包含一个与16S rRNA 3′结合的序列,CreT对tRNAucu的劫持抑制了一些关键基因的翻译,引起细菌毒性[30]。抗毒素CreA类似CRISPR-Cas系统的crRNA,通过引导Cas蛋白抑制CreT的转录[30]。CRISPR-Cas系统可利用抗毒素CreA控制毒素CreT的表达,使宿主菌无法丢失其CRISPR-Cas系统(对其“上瘾”)。一旦CRISPR-Cas组分被破坏,就会诱导CreT毒素的表达,从而抑制甚至杀死该宿主菌,从而保护了CRISPR-Cas系统在细胞群体中的稳定存在[30]。
2 TA的功能自从1983年发现TA可以通过分离后致死效应维持质粒和基因组的稳定以来,目前关于大部分TA的生物学功能还不清楚,甚至还有争议。经过四十年的发展,大量研究鉴定了一些新的TA,以及新的毒素活性和抗毒素的“解毒”机制,极大促进了我们对于TA的认识,目前已知的TA的功能至少包括以下几点。
2.1 调节质粒拷贝数TA最早被认为主要与质粒的分离后致死(post-segregational killing, PSK)有关,分离后致死主要依赖于TA中不稳定的抗毒素和能稳定存在的毒素发挥作用,当发生质粒丢失后,细菌无法持续产生抗毒素来中和细胞中的毒素,最终导致细胞死亡,因此确保存活下来的细菌中都含有携带TA的质粒[31]。大肠杆菌中发现的Ⅰ型TA中hok-sok系统和Ⅱ型TA中ccdAB系统[32],Ⅱ型TA中的parDE系统和kis/kid系统[33],部分Ⅲ型TA和Ⅳ型TA中的abiEi/ii都被证明具有稳定质粒复制的功能[34]。TA除了发挥PSK功能外,部分TA还可以通过直接调节质粒拷贝数,获得稳定遗传。最近研究发现Ⅱ型TA中PtpT/PrpA系统能调控质粒的复制过程,敲除PtpT/PrpA系统,不影响质粒的稳定性,反而质粒的拷贝数异常升高。最后发现抗毒素PrpA直接结合于质粒复制起始区的重复子序列,以浓度依赖的方式竞争阻碍质粒复制蛋白RepB对复制区的结合。在应激条件下,细菌中抗毒素发生降解,解除了质粒的复制抑制,质粒大量复制,保证了在不利环境下携带PtpT/PrpA系统的质粒稳定遗传。正常条件下,PtpT/PrpA系统对质粒复制进行抑制,避免了质粒的过度复制[35]。
2.2 促进持留菌与非可培养状态的形成持留菌是指代谢缓慢,表现出对抗生素和环境压力的高度耐受的细菌亚群[16]。持留菌同时是临床上一些感染性疾病反复发作的主要原因,关于持留菌的形成机制尚不完全清楚[36]。最近研究发现TA与持留菌的形成密切相关。最早在大肠杆菌中鉴定的与持留菌相关的TA是hipBA系统。该系统在应激环境下,RelA和SpoT (ppGpp合成酶)合成细胞内信号分子ppGpp,ppGpp能够抑制细胞中的去多聚磷酸酶(PPX),多聚磷酸激酶(PPK)则通过合成多聚磷酸(PolyP)活化Lon蛋白酶,Lon蛋白酶可以降解抗毒素,释放出HipA等毒素,从而抑制蛋白质的合成、DNA的复制等重要活动,最终抑制细菌生长,导致持留菌的形成[37]。随着抗毒素恢复至正常水平,毒素重新被抑制,细菌恢复活性。SOS反应也能够引起持留菌的形成,SOS反应是一种通过诱导某些Ⅰ型和Ⅱ型TA来应对氧化应激和抗生素作用的应激反应[38]。除此之外,沙门氏菌(Salmonella)毒素TacT通过乙酰化甘氨酰-tRNA,抑制蛋白质的合成,并促进持留菌的形成[39],研究发现当沙门氏菌中GNAT毒素基因被敲除以后,经巨噬细胞吞噬后,沙门氏菌形成的持留菌比例会大大降低[40]。当细菌遭遇不良生活环境时,如低温、高温、重金属、高渗透压、消毒剂、抗生素等,还会形成另一种活的非可培养的状态(VBNC),此时细菌仍具有代谢活性和完整的细胞结构,但在培养基上无法形成菌落[41]。细菌的VBNC状态与持留态联系紧密,相比于持留态下细菌短暂的休眠状态,VNBC状态是细菌一种更深层次的休眠状态[42]。目前发现TA系统的激活与微生物VBNC状态的形成密切相关,在不良环境下,TA触发系统中的relA、spoT、lon、ppx、ppk基因被激活,从而激活了相关TA系统,如:RelBE、HigBA、VapBC、MparDE2、HipBA等[42],TA系统中的抗毒素被降解,引起毒素抗毒素的比例失调,最终使得游离毒素含量增加[42]。游离的毒素通过抑制DNA复制及蛋白质翻译、促进mRNA断裂、抑制细胞分裂等促进微生物VBNC状态的形成[42]。
2.3 生物被膜的形成细菌细胞可以聚集在生物和非生物固体表面上,形成生物被膜。生物被膜是由胞外多糖基质包裹的多细胞聚合体[43],能帮助细菌对抗不利环境,并且表现出抗生素耐受性[44]。生物被膜还能帮助一些病原菌侵染宿主,如铜绿假单胞菌(Pseudomonas aeruginosa)通过形成生物被膜,对抗宿主的防御机制[45]。TA系统与生物被膜的形成密切相关[46],包括Ⅰ型TA系统sprG2-sprF2[47],Ⅱ型TA系统hicAB、prlF-yhaV和yafNO[48],Ⅴ型TA系统ghoST[49],Ⅶ型TA系统Hha-TomB[50],都被证明能够显著影响细菌生物被膜的形成。最早发现能够直接影响生物被膜形成的TA系统是mqsRA[51]。抗毒素MqsA是压力调节因子RpoS的阻遏物,而低浓度的RpoS则会降低GMP水平,最终限制生物被膜的形成。在应激条件下,Lon和ClpXP蛋白酶降解抗毒素MqsA,导致RpoS累积,最终使浮游细胞的高度运动状态转变为固着状态,从而形成生物被膜[51]。
2.4 抵御噬菌体感染目前关于TA功能比较明确的是参与抵御噬菌体侵染[12]。流产感染是通过在噬菌体复制阶段激活TA等方式,引起感染细胞的利他自杀,阻止噬菌体在细菌群体中的繁殖[52]。如大肠杆菌K-12 (Escherichia coli K-12)中发现的Ⅱ型TA系统中的rnlA-rnlB系统可以显著阻止T4噬菌体的感染,当噬菌体在大肠杆菌中复制时,会中断细菌细胞中一些基因的表达,其中包括抗毒素基因rnlB,并且细胞中抗毒素RnlB不稳定,容易降解,最终导致细胞中的毒素RnlA被释放出来,切割细胞中细菌和噬菌体的mRNA,从而抑制噬菌体在大肠杆菌内的增殖[53]。除此以外,Ⅲ型TA如toxIN和tenpIN家族,则能引起多种细菌的流产性感染,包括乳酸乳球菌(Lactococcus lactis)、发光光杆菌(Photorhabdus luminescens)和大肠杆菌。正常条件下,抗毒素ToxI能够与毒素蛋白ToxN形成稳定复合物,抑制毒素ToxN的活性。当噬菌体入侵细菌时,同样会引起抗毒素ToxI降解,毒素ToxN被释放,Ⅲ型TA系统中毒素ToxN也具有RNA酶活性,会切割细胞中的噬菌体和细菌的mRNA,最终导致细菌的死亡[54]。在噬菌体入侵时,已被证明具有抵抗作用的TA还包括Ⅰ型TA系统hok/sok[55]以及Ⅱ型TA系统MazEF[56]、DarTG[57]等,这些TA也能够通过激活其毒素毒性,杀死被噬菌体侵染的细菌,从而有效阻止噬菌体的侵染。此外,细菌的防御系统通常集中位于细菌的“防御岛”上,因此TA系统可能通过协同细菌其他防御系统,如CRISPR-Cas系统、限制性修复系统等,联合发挥抵抗噬菌体的功能[58]。
3 Ⅶ型TA的研究进展目前已经发现的Ⅶ型TA来自希瓦氏菌(Shewanella oneidensis)的HepT/MntA系统,结核分枝杆菌(Mycobacterium tuberculosis)中的Rv1045/Rv1044系统以及耶尔辛氏肠炎菌(Yersinia enterocolitica)中的Hha-TomB系统,如图 2所示。

|
| 图 2 Ⅶ型TA类型及其毒素中和机制 Figure 2 Summary of the type Ⅶ toxin/antitoxin (TA) systems in which the enzymatic antitoxin chemically modifies the toxin to neutralize it. |
3.1 HepT/MntA系统
HepT/MntA广泛存在于细菌和古菌中[59-60],通过细菌毒性实验验证了HepT/MntA作为一种新型TA,但毒素HEPN的底物仍不清楚[61]。鉴于HEPN的功能以及其他TA毒素的功能,猜测HEPN可能具有RNA酶功能,通过切割不同的RNA (tRNA、mRNA和rRNA)发现HEPN可以高效地切割ompA mRNA[61]。利用X-射线晶体学技术解析的HEPN/MNT复合物的结构,发现HEPN/MNT以6:2的比例形成一个异源八聚体,这不同于大多数TA 1:1的结合比例[29, 62]。HEPN通过二聚化形成一个V型的沟槽,其保守的RX4-6H酶活基序位于V型沟槽内,而MNT则主要与HEPN的α2和α4相互作用,对于中和HEPN的结合至关重要[29]。由于MNT可以通过与HEPN的直接相互作用中和其毒性,HEPN/MNT最初被认为是Ⅱ型TA[61]。但与Ⅱ型TA明显不同的是抗毒素MNT是一个具有核苷酸转移酶结构域的蛋白,而非Ⅱ型TA中抗毒素通常具有的转录因子结构域,此外,HEPN一个保守的R70对于HEPN/MNT的中和起到关键作用,而单独突变R70并不足以破坏HEPN/MNT的直接相互作用,这很难用Ⅱ型TA来解释[5]。
研究发现,HEPN/MNT共表达时,SDS-PAGE结果显示HEPN的分子量明显高于单独表达的HEPN (大约1 kD),将共表达的MNT保守的GSX10DXD结合位点突变后,HEPN分子量不再变大,这意味着毒素HEPN可能是被抗毒素MNT进行了某种修饰[29]。作为具有最小的核苷酸转移酶家族结构域的抗毒素MNT,该家族蛋白可以将核苷酸转移到具有羟基的氨基酸上,并与这个氨基酸上的羟基形成磷酸二酯键。随后通过HPLC/MS分析经PDE酶切后的HEPN的产物以及晶体结构,发现每个毒素HEPN的Y104被转移上了3个AMP,通过与HEPN未被腺苷酸化修饰的解耦股对比,发现Y104被腺苷酸化修饰导致了其RX4H loop向HEPN二聚体形成的沟槽外部发生了一个逆时针几乎180°的旋转[29]。并且这3个AMP紧贴着HEPN一个带正电荷的区域,包括HEPN一个高度保守的R70[61],因此,推测HEPN的腺苷酸化修饰可能占据了其与底物的结合位点。
同期研究关于蓝细菌(Aphanizomenon flos-aquae)中I-D CRISPR-Cas附近的一对HepT/MntA系统时,同样发现了类似现象,HEPN可以将tRNA 3′端切除4 nt,从而干扰蛋白质翻译过程,继而对细菌产生毒性,而MNT利用ATP将位于HEPN酶活loop的保守的Y109共价连接2个AMP,进而干扰蛋白质的翻译[63]。尽管在已经报道的HepT/MntA系统中,已经明确毒素的中和依赖于抗毒素对其腺苷酸化修饰,然而目前尚不清楚为什么其被修饰的数目不同,以及有没有其他未知因素将毒素上被修饰的腺苷酸去除[5]。
3.2 Hha-TomB系统Hha-TomB系统是存在于耶尔辛氏肠炎菌和大肠杆菌中的TA,大肠杆菌的Hha-TomB系统与生物被膜的形成有关,毒素Hha可以使大肠杆菌生物被膜的形成减少甚至导致细菌的裂解,而抗毒素Tom可以使Hha失去毒性[64]。最新研究发现抗毒素TomB可以将毒素Hha一个保守的半胱氨酸C18氧化成-SOXH,并导致毒素的稳定性降低,中和其毒性[65]。通过NMR解析了耶尔辛氏肠炎菌的抗毒素C117S YmoB的结构,发现它由一个包含4个反向平行的α螺旋和C末端的一个小α螺旋形成一个紧凑的结构,其中C117S位于C端的小α螺旋[65]。不同于Ⅱ型TA之间毒素与抗毒素形成紧密的复合物,通过15N标记的C117S YmoB发现Hha和TomB之间只是瞬时的相互作用,通过NMR发现TomB一个保守的E53对于Hha与TomB的互作很重要[66]。
3.3 Rv1045/Rv1044系统结核分枝杆菌是严重危害人类健康的一类病原菌,Rv0078A、Rv0836c、Rv1045和Rv2826a属于一类功能未知的DUF1814家族蛋白[67],它们都有一个核苷酸转移酶结构域(nucleotidyltransferase, NTase),NTase具有4个保守的motif,其中N端的Ⅰ和Ⅱ motif和DNA聚合酶具有类似的特征,可以通过与金属离子结合并负责核苷酸的转移,而C端的Ⅲ motif和tRNA核酸转移酶相似,可以在未成熟的tRNA 3′末端添加-CCA,而Ⅵ motif则可以通过与Ⅲ motif形成催化中心[68]。结核杆菌中4个DUF1814毒素蛋白都位于抗毒素蛋白的下游,其中Rv0078A上游的Rv0078B编码产物为68个氨基酸蛋白且与抗毒素MazE具有同源性,Rv0836c和COG4861基因组成一对TA,Rv1045和Rv2826c分别与Rv1044、Rv2827c组成TA,并且有研究表明Rv1044和Rv2827c对于结核分枝杆菌的生长十分关键[68]。
Rv1045/Rv1044 (|mycobacterial AbiE-like NTase toxins/antitoxin MenT3/MenA3|)最早被认为是Ⅳ型TA,Rv1045编码发挥毒素作用的鸟苷酸转移酶TglT (unusual type guanylytransferase-like toxin),而Rv1044编码发挥抗毒素功能的丝氨酸蛋白激酶TakA (unusual type of atypical kinase antitoxin)[67]。Rv1045作为一个具有鸟苷转移酶活性的毒素,可以结合NTP,例如ATP、GTP、CTP等,特别对于GTP具有偏好性[67]。Rv1045对大肠杆菌的生长抑制可以被Rv1044解除,然而Rv1045和Rv1044之间可以直接相互作用,这不同于Ⅳ型TA。Rv1045高分辨率的结构显示它的整体结构呈双叶状,由N-端结构域(N-terminal domain, NTD)和C-端结构域(C-terminal domain, CTD)组成,其中N端结构域由一个核苷转移酶家族蛋白典型的α/β折叠,而C端结构域由5个α螺旋组成,NTD和CTD之间有一个腔,保守的D80、D82和E146位于NTD和CTD之间的腔中,此外,这个腔还富含一些带正电的氨基酸,它们可能参与和GTP的结合[67]。
有趣的是Rv1045一个保守的S78位点发现被磷酸化修饰,并且其磷酸化依赖于上游的Rv1044[67]。由于Rv1044缺乏激酶的典型特征被认为是一个非典型的激酶,通过HHpred分析发现Rv1045和Rv2827c都包含一个N端的HTH结构域和C端一个未知功能的结构域,将其保守的G71和D74突变后,放射性自显影发现Rv1044则不能对Rv1045进行磷酸化修饰[67]。然而,Rv1045与GTP的复合物结构也未见报道,S78修饰后的Rv1045如何抑制细菌生长的分子机制目前仍不清楚。体外等温滴定量热法发现磷酸化的Rv1045对GTP的结合能力显著低于未磷酸化的Rv1045,推测抗毒素Rv1044对毒素Rv1045的磷酸化阻止了其对GTP的结合[67]。虽然Rv1044和Rv1045之间有直接的相互作用,但是目前Rv1044-Rv1045复合物的结构尚未报道,对于Rv1044磷酸化修饰Rv1045的分子机制也不清楚[67]。
尽管目前已发现的3种Ⅶ型TA的中和机制几乎同时被揭示,但仍有一些问题没有被解决。如,Ⅶ型TA是否从代谢酶进化而来,Ⅶ型TA在细菌中是否发挥着更多的生物学功能,以及在细菌中是否存在着另外的途径能够逆转Ⅶ型TA的翻译后修饰?HepT/MntA和MenT/MenA (Rv1045/Rv1044)中的抗毒素都属于NTase家族蛋白,却可以对毒素分别进行腺苷酸化修饰和磷酸化修饰,细菌中广泛存在着翻译后修饰,那么在细菌中是否存在着更多新的Ⅶ型TA和新的中和机制?这些都是在后续研究中需要解决的问题。Ⅶ型TA能够在致病菌中发挥稳定的翻译后修饰,通过采取抑制抗毒素的表达或破坏抗毒素对毒素的翻译后修饰的方式,使毒素发挥毒性,从而抑制细菌生长。这也说明了Ⅶ型TA作为新型TA,在耐药菌的治疗和药物靶点的选择上有着巨大的潜力以及应用前景。
4 TA毒素作用位点TA系统参与了细菌细胞中的许多重要过程,包括DNA复制、转录、蛋白质翻译、细胞壁合成以及细胞骨架的形成,如图 3所示。部分毒素能够靶向切割mRNA,以大肠杆菌中的Ⅱ型TA中的mazEF系统为例,mazEF系统的毒素为特异性的核糖核酸内切酶,能特异性切割mRNA的5′-ACA-3′上游的碱基[69],类似的还有VapC和RelE毒素。部分MazF毒素表现为作用于23S rRNA、16S rRNA和tRNA,从而抑制翻译[70]。HicA毒素具有特异性双链RNA结合域(~50个氨基酸)能水解RNA[71]。而RelE毒素能在核糖体A位点mRNA密码子第2位和第3位之间切割。RelE家族的毒素具有低序列同源性,但保留类似于T1、SA2和U2 (核糖体非依赖性核糖核酸内切酶)的保守折叠[72]。

|
| 图 3 TA系统毒素作用位点 Figure 3 The molecular targets of TA system encoded toxins. |
大部分TA发挥功能都是通过干扰蛋白质的合成,由于蛋白质翻译是一个复杂的过程,包括核糖体的组装和氨基酸逐个添加到新生的多肽链中,目前发现毒素可以在蛋白质合成的各个步骤发挥作用[13]。例如Ⅱ型TA通过多种方式干扰翻译,从翻译前和翻译过程中mRNA转录物的切割,到tRNA结合氨基酸或肽链的延伸。一些毒素还可以通过干扰翻译机制来阻止蛋白质的合成。例如,谷氨酸tRNA合成酶被HipA毒素磷酸化,导致蛋白质合成受到抑制[37]。phd-Doc系统的毒素Doc通过磷酸化保守的关键位点,导致EF-Tu失活[73]。VapBC系统的VapC毒素识别并切割起始tRNA (tRNAfMet)、特异性tRNA和23S rRNA的SRL[74]。AtaT和TacT是新发现的具有乙酰转移酶活性的毒素[75],毒素AtaT通过乙酰化起始tRNA上结合的蛋氨酸来抑制翻译起始而毒素TacT能够乙酰化tRNA的延伸因子。毒素MbcT具有NAD磷酸化酶活性,能够通过磷酸化,耗尽细胞内的NAD,导致细胞死亡[76],同家族的毒素ParT通过ADP-核糖基化磷酸核糖焦磷酸合成酶,从而抑制蛋白质合成[77]。而另一种具有ADP核糖基转移酶活性的Ⅳ型TA的毒素DarT则通过ADP核糖基化单链DNA抑制DNA复制[78]。
Ⅱ型TA以外的TA系统的作用机制,到目前为止还未研究十分透彻。其他类型的部分TA,如Ⅰ型TA中Hok毒素使细胞膜去极化,导致细胞损伤[79]。最近Ⅲ型TA复合物的研究表明,毒素ToxN具有核糖核酸内切酶功能,在细胞内切割序列为AA↓AU,GAA↓AU和AAA↓AA[23]的RNA。Ⅳ型TA中CbtA毒素可阻止细胞骨架蛋白(MreB和FtsZ)的聚合[25]。V型TA中GhoT毒素能破坏细胞膜,导致细胞溶解[27]。Ⅵ型TA中SocB毒素在DNA复制过程中,与DNA聚合酶竞争性结合β夹子,阻止DNA复制[28]。在Ⅶ型TA中,Hha毒素是一种血溶素表达调节蛋白,过表达后可导致细胞溶解[66]。在Ⅷ型TA,毒素CreT RNA不仅可以通过稀有密码子劫持稀有氨基酸精氨酸tRNAUCU,还可以劫持异亮氨酸tRNACAU发挥毒性,进而抑制其他重要蛋白的合成[30, 80]。
一些TA系统的毒素之间存在共同的作用位点,例如CcdB和ParE共同作用于DNA旋转酶,结合DNA旋转酶的亚基可阻断DNA聚合酶的通道,抑制DNA的复制[81]。非传统的三元ω-ε-ζTA系统的zeta毒素的作用,通过磷酸化必需核苷酸糖UDP-N-乙酰氨基葡萄糖来抑制细胞壁合成[82]。
5 总结与讨论由于TA存在于所有的细菌、古细菌以及原噬菌体中,研究发现TA与微生物的致病性密切相关,特别是在致病微生物中分布尤为丰富,因此,TA的鉴定、中和机制以及致病机理引起了许多微生物学家以及医药学界的关注。尤其是抗毒素可以特异性中和毒素对细菌的毒性,基于这一点,不少研究认为这为以毒素-抗毒素为靶标的抗菌药物设计提供了新思路。同时可以利用TA维持质粒稳定性、切割核酸等的特点,开发新的基因工程和分子生物学工具。研究表明,TA还可以应用在临床上,在抗肿瘤和抗病毒的治疗中有着重要意义[13]。并且目前发现的基于翻译后修饰的Ⅶ型TA广泛存在于结核杆菌、幽门螺杆菌等致病微生物中,并对它们的致病力起到重要作用。因此,对它们的致病机制的深入研究以及中和机理的研究,可以为后续这些微生物的防治提供更多选择。
随着对TA不断深入的研究,虽然越来越多的新型TA及其作用机制被发现,例如最近在嗜肺军团菌中发现丝/苏氨酸激酶效应蛋白Lpg2370与同一操纵子下的上游2个蛋白组成三元HipBST TA,其中毒素HipT兼具效应蛋白功能[83],此外,水稻百叶枯病菌效应蛋白AvrRxo1-ORF1也与下游的AvrRxo1-ORF2形成TA[84],其中毒素AvrRxo1-ORF1在病原菌感染时可以抑制维生素B6的生物合成[85],意味着TA可能与效应蛋白从进化上有某种联系。总之,TA作为一个广泛存在于微生物的遗传元件,对于TA的生物学功能急需深入研究。对于TA的深入研究,还能进一步促进生物技术的发展以及解决耐药菌的难题。
| [1] | HARMS A, BRODERSEN DE, MITARAI N, GERDES K. Toxins, targets, and triggers: an overview of toxin-antitoxin biology. Molecular Cell, 2018, 70(5): 768-784. DOI:10.1016/j.molcel.2018.01.003 |
| [2] | PAGE R, PETI W. Toxin-antitoxin systems in bacterial growth arrest and persistence. Nature Chemical Biology, 2016, 12(4): 208-214. DOI:10.1038/nchembio.2044 |
| [3] | CAVAILLON JM. Historical links between toxinology and immunology[J]. Pathogens and Disease, 2018, 76(3): 10.1093/femspd/fty019. |
| [4] | KAMRUZZAMAN M, WU AY, IREDELL JR. Biological functions of type Ⅱ toxin-antitoxin systems in bacteria. Microorganisms, 2021, 9(6): 1276. DOI:10.3390/microorganisms9061276 |
| [5] | WANG XX, YAO JY, SUN YC, WOOD TK. Type Ⅶ toxin/antitoxin classification system for antitoxins that enzymatically neutralize toxins. Trends in Microbiology, 2021, 29(5): 388-393. DOI:10.1016/j.tim.2020.12.001 |
| [6] | CHOI JS, KIM W, SUK S, PARK H, BAK G, YOON J, LEE Y. The small RNA, SdsR, acts as a novel type of toxin in Escherichia coli. RNA Biology, 2018, 15(10): 1319-1335. DOI:10.1080/15476286.2018.1532252 |
| [7] | SONG S, WOOD TK. Toxin/antitoxin system paradigms: toxins bound to antitoxins are not likely activated by preferential antitoxin degradation. Advanced Biosystems, 2020, 4(3): e1900290. DOI:10.1002/adbi.201900290 |
| [8] | JURĖNAS D, FRAIKIN N, GOORMAGHTIGH F, van MELDEREN L. Biology and evolution of bacterial toxin-antitoxin systems. Nature Reviews Microbiology, 2022, 20(6): 335-350. DOI:10.1038/s41579-021-00661-1 |
| [9] | BRIELLE R, PINEL-MARIE ML, FELDEN B. Linking bacterial type I toxins with their actions. Current Opinion in Microbiology, 2016, 30: 114-121. DOI:10.1016/j.mib.2016.01.009 |
| [10] | GERDES K, BECH FW, JØRGENSEN ST, LØBNER-OLESEN A, RASMUSSEN PB, ATLUNG T, BOE L, KARLSTROM O, MOLIN S, von MEYENBURG K. Mechanism of postsegregational killing by the hok gene product of the parB system of plasmid R1 and its homology with the relF gene product of the E. coli relB operon. The EMBO Journal, 1986, 5(8): 2023-2029. DOI:10.1002/j.1460-2075.1986.tb04459.x |
| [11] | WAGNER EGH, UNOSON C. The toxin-antitoxin system tisB-istR1: expression, regulation, and biological role in persister phenotypes. RNA Biology, 2012, 9(12): 1513-1519. DOI:10.4161/rna.22578 |
| [12] | LEROUX M, LAUB MT. Toxin-antitoxin systems as phage defense elements. Annual Review of Microbiology, 2022, 76: 21-43. DOI:10.1146/annurev-micro-020722-013730 |
| [13] | SINGH G, YADAV M, GHOSH C, RATHORE JS. Bacterial toxin-antitoxin modules: classification, functions, and association with persistence. Current Research in Microbial Sciences, 2021, 2: 100047. DOI:10.1016/j.crmicr.2021.100047 |
| [14] | GOEDERS N, van MELDEREN L. Toxin-antitoxin systems as multilevel interaction systems. Toxins, 2014, 6(1): 304-324. DOI:10.3390/toxins6010304 |
| [15] | COUSSENS NP, DAINES DA. Wake me when it՚s over-bacterial toxin-antitoxin proteins and induced dormancy. Experimental Biology and Medicine: Maywood, N J, 2016, 241(12): 1332-1342. DOI:10.1177/1535370216651938 |
| [16] | GERDES K, MAISONNEUVE E. Bacterial persistence and toxin-antitoxin loci. Annual Review of Microbiology, 2012, 66: 103-123. DOI:10.1146/annurev-micro-092611-150159 |
| [17] | CATAUDELLA I, TRUSINA A, SNEPPEN K, GERDES K, MITARAI N. Conditional cooperativity in toxin-antitoxin regulation prevents random toxin activation and promotes fast translational recovery. Nucleic Acids Research, 2012, 40(14): 6424-6434. DOI:10.1093/nar/gks297 |
| [18] | WOOD TL, WOOD TK. The HigB/HigA toxin/antitoxin system of Pseudomonas aeruginosa influences the virulence factors pyochelin, pyocyanin, and biofilm formation. MicrobiologyOpen, 2016, 5(3): 499-511. DOI:10.1002/mbo3.346 |
| [19] | CHAN WT, NIETO C, HARIKRISHNA JA, KHOO SK, OTHMAN RY, ESPINOSA M, YEO CC. Genetic regulation of the yefM-yoeB toxin-antitoxin locus of Streptococcus pneumoniae. Journal of Bacteriology, 2011, 193(18): 4612-4625. DOI:10.1128/JB.05187-11 |
| [20] | YAMAGUCHI Y, PARK JH, INOUYE M. MqsR, a crucial regulator for quorum sensing and biofilm formation, is a GCU-specific mRNA interferase in Escherichia coli. The Journal of Biological Chemistry, 2009, 284(42): 28746-28753. DOI:10.1074/jbc.M109.032904 |
| [21] | LEWIS K. Multidrug tolerance of biofilms and persister cells. Current Topics in Microbiology and Immunology, 2008, 322: 107-131. |
| [22] | FINERAN PC, BLOWER TR, FOULDS IJ, HUMPHREYS DP, LILLEY KS, SALMOND GPC. The phage abortive infection system, ToxIN, functions as a protein-RNA toxin-antitoxin pair. Proceedings of the National Academy of Sciences of the United States of America, 2009, 106(3): 894-899. DOI:10.1073/pnas.0808832106 |
| [23] | MANIKANDAN P, SANDHYA S, NADIG K, PAUL S, SRINIVASAN N, ROTHWEILER U, SINGH M. Identification, functional characterization, assembly and structure of ToxIN type Ⅲ toxin-antitoxin complex from E. coli. Nucleic Acids Research, 2022, 50(3): 1687-1700. DOI:10.1093/nar/gkab1264 |
| [24] | BLOWER TR, FINERAN PC, JOHNSON MJ, TOTH IK, HUMPHREYS DP, SALMOND GPC. Mutagenesis and functional characterization of the RNA and protein components of the toxIN abortive infection and toxin-antitoxin locus of Erwinia. Journal of Bacteriology, 2009, 191(19): 6029-6039. DOI:10.1128/JB.00720-09 |
| [25] | MASUDA H, TAN Q, AWANO N, WU KP, INOUYE M. YeeU enhances the bundling of cytoskeletal polymers of MreB and FtsZ, antagonizing the CbtA (YeeV) toxicity in Escherichia coli. Molecular Microbiology, 2012, 84(5): 979-989. DOI:10.1111/j.1365-2958.2012.08068.x |
| [26] | HELLER DM, TAVAG M, HOCHSCHILD A. CbtA toxin of Escherichia coli inhibits cell division and cell elongation via direct and independent interactions with FtsZ and MreB. PLoS Genetics, 2017, 13(9): e1007007. DOI:10.1371/journal.pgen.1007007 |
| [27] | WANG XX, LORD DM, CHENG HY, OSBOURNE DO, HONG SH, SANCHEZ-TORRES V, QUIROGA C, ZHENG K, HERRMANN T, PETI W, et al. A new type Ⅴ toxin-antitoxin system where mRNA for toxin GhoT is cleaved by antitoxin GhoS. Nature Chemical Biology, 2012, 8(10): 855-861. DOI:10.1038/nchembio.1062 |
| [28] | AAKRE CD, PHUNG TN, HUANG D, LAUB MT. A bacterial toxin inhibits DNA replication elongation through a direct interaction with the β sliding clamp. Molecular Cell, 2013, 52(5): 617-628. DOI:10.1016/j.molcel.2013.10.014 |
| [29] | YAO JY, ZHEN XK, TANG KH, LIU TL, XU XL, CHEN Z, GUO YX, LIU XX, WOOD TK, OUYANG SY, WANG XX. Novel polyadenylylation-dependent neutralization mechanism of the HEPN/MNT toxin/antitoxin system. Nucleic Acids Research, 2020, 48(19): 11054-11067. DOI:10.1093/nar/gkaa855 |
| [30] | LI M, GONG LY, CHENG FY, YU HY, ZHAO DH, WANG R, WANG T, ZHANG SJ, ZHOU J, SHMAKOV SA, KOONIN EV, XIANG H. Toxin-antitoxin RNA pairs safeguard CRISPR-Cas systems. Science, 2021, 372(6541): eabe5601. DOI:10.1126/science.abe5601 |
| [31] | KARLOWICZ A, WEGRZYN K, DUBIEL A, ROPELEWSKA M, KONIECZNY I. Proteolysis in plasmid DNA stable maintenance in bacterial cells. Plasmid, 2016, 86: 7-13. DOI:10.1016/j.plasmid.2016.05.002 |
| [32] | GERDES K, RASMUSSEN PB, MOLIN S. Unique type of plasmid maintenance function: postsegregational killing of plasmid-free cells. Proceedings of the National Academy of Sciences of the United States of America, 1986, 83(10): 3116-3120. DOI:10.1073/pnas.83.10.3116 |
| [33] | ROBERTS RC, STRÖM AR, HELINSKI DR. The parDE operon of the broad-host-range plasmid RK2 specifies growth inhibition associated with plasmid loss. Journal of Molecular Biology, 1994, 237(1): 35-51. DOI:10.1006/jmbi.1994.1207 |
| [34] | DY RL, PRZYBILSKI R, SEMEIJN K, SALMOND GPC, FINERAN PC. A widespread bacteriophage abortive infection system functions through a type Ⅳ toxin-antitoxin mechanism. Nucleic Acids Research, 2014, 42(7): 4590-4605. DOI:10.1093/nar/gkt1419 |
| [35] | NI SW, LI BY, TANG KH, YAO JY, WOOD TK, WANG PX, WANG XX. Conjugative plasmid-encoded toxin-antitoxin system PrpT/PrpA directly controls plasmid copy number. Proceedings of the National Academy of Sciences of the United States of America, 2021, 118(4): e2011577118. DOI:10.1073/pnas.2011577118 |
| [36] | ZOU J, PENG B, QU JX, ZHENG J. Are bacterial persisters dormant cells only?. Frontiers in Microbiology, 2022, 12: 708580. DOI:10.3389/fmicb.2021.708580 |
| [37] | GERMAIN E, CASTRO-ROA D, ZENKIN N, GERDES K. Molecular mechanism of bacterial persistence by HipA. Molecular Cell, 2013, 52(2): 248-254. DOI:10.1016/j.molcel.2013.08.045 |
| [38] | FRAIKIN N, GOORMAGHTIGH F, van MELDEREN L. Type Ⅱ toxin-antitoxin systems: evolution and revolutions. Journal of Bacteriology, 2020, 202(7): e00763-e00719. |
| [39] | YASHIRO Y, ZHANG CQ, SAKAGUCHI Y, SUZUKI T, TOMITA K. Molecular basis of glycyl-tRNAGly acetylation by TacT from Salmonella typhimurium. Cell Reports, 2021, 37(12): 110130. DOI:10.1016/j.celrep.2021.110130 |
| [40] | CHEVERTON AM, GOLLAN B, PRZYDACZ M, WONG CT, MYLONA A, HARE SA, HELAINE S. A Salmonella toxin promotes persister formation through acetylation of tRNA. Molecular Cell, 2016, 63(1): 86-96. DOI:10.1016/j.molcel.2016.05.002 |
| [41] | LIU JY, DENG Y, LI L, LI B, LI YY, ZHOU SS, SHIRTLIFF ME, XU ZB, PETERS BM. Discovery and control of culturable and viable but non-culturable cells of a distinctive Lactobacillus harbinensis strain from spoiled beer. Scientific Reports, 2018, 8(1): 11446. DOI:10.1038/s41598-018-28949-y |
| [42] |
ZHANG TH, MENG LL, ZHAO F. Progress in research on the effect of toxin-antitoxin systems on the formation of the viable but non-culturable state of microorganisms. Food Science, 2022, 43(15): 275-282.
(in Chinese) 张铁华, 孟玲玲, 赵凤. 毒素-抗毒素系统对微生物活的非可培养状态形成的影响研究进展. 食品科学, 2022, 43(15): 275-282. DOI:10.7506/spkx1002-6630-20220316-185 |
| [43] | LIMOLI DH, JONES CJ, WOZNIAK DJ. Bacterial extracellular polysaccharides in biofilm formation and function[J]. Microbiology Spectrum, 2015, 3(3): 10.1128/microbiolspec. MB-10.1128/microbiolspe0011-2014. |
| [44] | SINGH S, SINGH SK, CHOWDHURY I, SINGH R. Understanding the mechanism of bacterial biofilms resistance to antimicrobial agents. The Open Microbiology Journal, 2017, 11: 53-62. DOI:10.2174/1874285801711010053 |
| [45] | KUMAR S, ENGELBERG-KULKA H. Quorum sensing peptides mediating interspecies bacterial cell death as a novel class of antimicrobial agents. Current Opinion in Microbiology, 2014, 21: 22-27. DOI:10.1016/j.mib.2014.09.001 |
| [46] | MERFA MV, NIZA B, TAKITA MA, de SOUZA AA. The MqsRA toxin-antitoxin system from Xylella fastidiosa plays a key role in bacterial fitness, pathogenicity, and persister cell formation. Frontiers in Microbiology, 2016, 7: 904. |
| [47] | ORIOL C, CENGHER L, MANNA AC, MAURO T, PINEL-MARIE ML, FELDEN B, CHEUNG A, ROUILLON A. Expanding the Staphylococcus aureus SarA regulon to small RNAs. mSystems, 2021, 6(5): e0071321. DOI:10.1128/mSystems.00713-21 |
| [48] |
HOU B, WANG CY, ZHOU LJ. The roles and regulatory mechanism of toxin-antitoxin system in bacterial biofilm formation[J/OL]. Acta Veterinaria et Zootechnica Sinica, 2022: 1-12. (2022-07-22).https://kns.cnki.net/kcms/detail/11.1985.S.20220721.1136.002.html (in Chinese). 侯博, 王晨燕, 周伦江. 毒素-抗毒素系统在细菌生物被膜形成中的作用及调控机制[J/OL]. 畜牧兽医学报, 2022: 1-12. (2022-07-22).https://kns.cnki.net/kcms/detail/11.1985.S.20220721.1136.002.html. |
| [49] | WANG XX, LORD DM, HONG SH, PETI W, BENEDIK MJ, PAGE R, WOOD TK. Type Ⅱ toxin/antitoxin MqsR/MqsA controls type V toxin/antitoxin GhoT/GhoS. Environmental Microbiology, 2013, 15(6): 1734-1744. DOI:10.1111/1462-2920.12063 |
| [50] | GARCÍA-CONTRERAS R, ZHANG XS, KIM Y, WOOD TK. Protein translation and cell death: the role of rare tRNAs in biofilm formation and in activating dormant phage killer genes. PLoS One, 2008, 3(6): e2394. DOI:10.1371/journal.pone.0002394 |
| [51] | SOO VWC, WOOD TK. Antitoxin MqsA represses curli formation through the master biofilm regulator CsgD. Scientific Reports, 2013, 3: 3186. DOI:10.1038/srep03186 |
| [52] | DY RL, RICHTER C, SALMOND GPC, FINERAN PC. Remarkable mechanisms in microbes to resist phage infections. Annual Review of Virology, 2014, 1(1): 307-331. DOI:10.1146/annurev-virology-031413-085500 |
| [53] | KOGA M, OTSUKA Y, LEMIRE S, YONESAKI T. Escherichia coli rnlA and rnlB compose a novel toxin-antitoxin system. Genetics, 2011, 187(1): 123-130. DOI:10.1534/genetics.110.121798 |
| [54] | GOEDERS N, CHAI R, CHEN BH, DAY A, SALMOND GPC. Structure, evolution, and functions of bacterial type Ⅲ toxin-antitoxin systems. Toxins, 2016, 8(10): 282. DOI:10.3390/toxins8100282 |
| [55] | PECOTA DC, WOOD TK. Exclusion of T4 phage by the hok/sok killer locus from plasmid R1. Journal of Bacteriology, 1996, 178(7): 2044-2050. DOI:10.1128/jb.178.7.2044-2050.1996 |
| [56] | HAZAN R, ENGELBERG-KULKA H. Escherichia coli mazEF-mediated cell death as a defense mechanism that inhibits the spread of phage P1. Molecular Genetics and Genomics, 2004, 272(2): 227-234. DOI:10.1007/s00438-004-1048-y |
| [57] | LEROUX M, SRIKANT S, TEODORO GIC, ZHANG T, LITTLEHALE ML, DORON S, BADIEE M, LEUNG AKL, SOREK R, LAUB MT. The DarTG toxin-antitoxin system provides phage defence by ADP-ribosylating viral DNA. Nature Microbiology, 2022, 7(7): 1028-1040. DOI:10.1038/s41564-022-01153-5 |
| [58] |
HAI Y, WANG XY, XIE JP. The role of bacterial toxin-antitoxin systems in phage abortive infections. Chinese Journal of Biotechnology, 2022, 38(9): 3291-3300.
(in Chinese) 海洋, 王小雨, 谢建平. 细菌毒素-抗毒素系统在噬菌体流产感染中的作用. 生物工程学报, 2022, 38(9): 3291-3300. DOI:10.13345/j.cjb.220140 |
| [59] | MAKAROVA KS, WOLF YI, KOONIN EV. Comprehensive comparative-genomic analysis of type 2 toxin-antitoxin systems and related mobile stress response systems in prokaryotes. Biology Direct, 2009, 4: 19. DOI:10.1186/1745-6150-4-19 |
| [60] | SBERRO H, LEAVITT A, KIRO R, KOH E, PELEG Y, QIMRON U, SOREK R. Discovery of functional toxin/antitoxin systems in bacteria by shotgun cloning. Molecular Cell, 2013, 50(1): 136-148. DOI:10.1016/j.molcel.2013.02.002 |
| [61] | YAO JY, GUO YX, ZENG ZS, LIU XX, SHI F, WANG XX. Identification and characterization of a HEPN-MNT family type Ⅱ toxin-antitoxin in Shewanella oneidensis. Microbial Biotechnology, 2015, 8(6): 961-973. DOI:10.1111/1751-7915.12294 |
| [62] | JIA XY, YAO JY, GAO ZQ, LIU GF, DONG YH, WANG XX, ZHANG H. Structure-function analyses reveal the molecular architecture and neutralization mechanism of a bacterial HEPN-MNT toxin-antitoxin system. Journal of Biological Chemistry, 2018, 293(18): 6812-6823. DOI:10.1074/jbc.RA118.002421 |
| [63] | SONGAILIENE I, JUOZAPAITIS J, TAMULAITIENE G, RUKSENAITE A, ŠULČIUS S, SASNAUSKAS G, VENCLOVAS Č, SIKSNYS V. HEPN-MNT toxin-antitoxin system: the HEPN ribonuclease is neutralized by OligoAMPylation. Molecular Cell, 2020, 80(6): 955-970.e7. DOI:10.1016/j.molcel.2020.11.034 |
| [64] | JAISWAL S, PAUL P, PADHI C, RAY S, RYAN D, DASH S, SUAR M. The hha-TomB toxin-antitoxin system shows conditional toxicity and promotes persister cell formation by inhibiting apoptosis-like death in S. typhimurium. Scientific Reports, 2016, 6: 38204. DOI:10.1038/srep38204 |
| [65] | MARIMON O, TEIXEIRA JMC, CORDEIRO TN, SOO VWC, WOOD TL, MAYZEL M, AMATA I, GARCÍA J, MORERA A, GAY M, VILASECA M, OREKHOV VY, WOOD TK, PONS M. An oxygen-sensitive toxin-antitoxin system. Nature Communications, 2016, 7: 13634. DOI:10.1038/ncomms13634 |
| [66] | BARRIOS AF, ZUO RJ, REN DC, WOOD TK. Hha, YbaJ, and OmpA regulate Escherichia coli K12 biofilm formation and conjugation plasmids abolish motility. Biotechnology and Bioengineering, 2006, 93(1): 188-200. DOI:10.1002/bit.20681 |
| [67] | YU X, GAO XP, ZHU KX, YIN H, MAO XJ, WOJDYLA JA, QIN B, HUANG HR, WANG MT, SUN YC, CUI S. Characterization of a toxin-antitoxin system in Mycobacterium tuberculosis suggests neutralization by phosphorylation as the antitoxicity mechanism. Communications Biology, 2020, 3(1): 216. DOI:10.1038/s42003-020-0941-1 |
| [68] | CAI YM, USHER B, GUTIERREZ C, TOLCAN A, MANSOUR M, FINERAN PC, CONDON C, NEYROLLES O, GENEVAUX P, BLOWER TR. A nucleotidyltransferase toxin inhibits growth of Mycobacterium tuberculosis through inactivation of tRNA acceptor stems. Science Advances, 2020, 6(31): eabb6651. DOI:10.1126/sciadv.abb6651 |
| [69] | MUÑOZ-GÓMEZ AJ, SANTOS-SIERRA S, BERZAL-HERRANZ A, LEMONNIER M, DÍAZ-OREJAS R. Insights into the specificity of RNA cleavage by the Escherichia coli MazF toxin. FEBS Letters, 2004, 567(2/3): 316-320. |
| [70] | SCHIFANO JM, CRUZ JW, VVEDENSKAYA IO, EDIFOR R, OUYANG M, HUSSON RN, NICKELS BE, WOYCHIK NA. tRNA is a new target for cleavage by a MazF toxin. Nucleic Acids Research, 2016, 44(3): 1256-1270. DOI:10.1093/nar/gkv1370 |
| [71] | JØRGENSEN MG, PANDEY DP, JASKOLSKA M, GERDES K. HicA of Escherichia coli defines a novel family of translation-independent mRNA interferases in bacteria and archaea. Journal of Bacteriology, 2009, 191(4): 1191-1199. DOI:10.1128/JB.01013-08 |
| [72] | NEUBAUER C, GAO YG, ANDERSEN KR, DUNHAM CM, KELLEY AC, HENTSCHEL J, GERDES K, RAMAKRISHNAN V, BRODERSEN DE. The structural basis for mRNA recognition and cleavage by the ribosome-dependent endonuclease RelE. Cell, 2009, 139(6): 1084-1095. DOI:10.1016/j.cell.2009.11.015 |
| [73] | CRUZ JW, ROTHENBACHER FP, MAEHIGASHI T, LANE WS, DUNHAM CM, WOYCHIK NA. Doc toxin is a kinase that inactivates elongation factor Tu. Journal of Biological Chemistry, 2014, 289(28): 19276. DOI:10.1074/jbc.A113.544429 |
| [74] | WINTHER K, TREE JJ, TOLLERVEY D, GERDES K. VapCs of Mycobacterium tuberculosis cleave RNAs essential for translation. Nucleic Acids Research, 2016, 44(20): 9860-9871. DOI:10.1093/nar/gkw781 |
| [75] | JURĖNAS D, GARCIA-PINO A, van MELDEREN L. Novel toxins from type Ⅱ toxin-antitoxin systems with acetyltransferase activity. Plasmid, 2017, 93: 30-35. DOI:10.1016/j.plasmid.2017.08.005 |
| [76] | FREIRE DM, GUTIERREZ C, GARZA-GARCIA A, GRABOWSKA AD, SALA AJ, ARIYACHAOKUN K, PANIKOVA T, BECKHAM KSH, COLOM A, POGENBERG V, CIANCI M, TUUKKANEN A, BOUDEHEN YM, PEIXOTO A, BOTELLA L, SVERGUN DI, SCHNAPPINGER D, SCHNEIDER TR, GENEVAUX P, de CARVALHO LPS, et al. An NAD+ phosphorylase toxin triggers Mycobacterium tuberculosis cell death. Molecular Cell, 2019, 73(6): 1282-1291.e8. DOI:10.1016/j.molcel.2019.01.028 |
| [77] | PISCOTTA FJ, JEFFREY PD, LINK AJ. ParST is a widespread toxin-antitoxin module that targets nucleotide metabolism. Proceedings of the National Academy of Sciences of the United States of America, 2019, 116(3): 826-834. DOI:10.1073/pnas.1814633116 |
| [78] | HARMS A, GERDES K. Back to the roots: deep view into the evolutionary history of ADP-ribosylation opened by the DNA-targeting toxin-antitoxin module DarTG. Molecular Cell, 2016, 64(6): 1020-1021. DOI:10.1016/j.molcel.2016.11.038 |
| [79] | JAHN N, BRANTL S, STRAHL H. Against the mainstream: the membrane-associated type Ⅰ toxin BsrG from Bacillus subtilisinterferes with cell envelope biosynthesis without increasing membrane permeability. Molecular Microbiology, 2015, 98(4): 651-666. DOI:10.1111/mmi.13146 |
| [80] | CHENG FY, WANG R, YU HY, LIU C, YANG J, XIANG H, LI M. Divergent degeneration of creA antitoxin genes from minimal CRISPRs and the convergent strategy of tRNA-sequestering CreT toxins. Nucleic Acids Research, 2021, 49(18): 10677-10688. DOI:10.1093/nar/gkab821 |
| [81] | KOHANSKI MA, DWYER DJ, COLLINS JJ. How antibiotics kill bacteria: from targets to networks. Nature Reviews Microbiology, 2010, 8(6): 423-435. DOI:10.1038/nrmicro2333 |
| [82] | ÁLAMO MMD, TABONE M, MUÑOZ-MARTÍNEZ J, VALVERDE JR, ALONSO JC. Toxin ζ reduces the ATP and modulates the uridine diphosphate-N-acetylglucosamine pool. Toxins, 2019, 11(1): 29. DOI:10.3390/toxins11010029 |
| [83] | ZHEN XK, WU YY, GE JL, FU JQ, YE L, LIN NN, HUANG ZJ, LIU ZH, LUO ZQ, QIU JZ, OUYANG SY. Molecular mechanism of toxin neutralization in the HipBST toxin-antitoxin system of Legionella pneumophila. Nature Communications, 2022, 13(1): 4333. DOI:10.1038/s41467-022-32049-x |
| [84] | HAN Q, ZHOU CH, WU SC, LIU Y, TRIPLETT L, MIAO JM, TOKUHISA J, DEBLAIS L, ROBINSON H, LEACH JE, LI JY, ZHAO BY. Crystal structure of Xanthomonas AvrRxo1-ORF1, a type Ⅲ effector with a polynucleotide kinase domain, and its interactor AvrRxo1-ORF2. Structure, 2015, 23(10): 1900-1909. DOI:10.1016/j.str.2015.06.030 |
| [85] | LIU HF, LU CC, LI Y, WU T, ZHANG BG, LIU BY, FENG WJ, XU Q, DONG HS, HE SY, CHU ZH, DING XH. The bacterial effector AvrRxo1 inhibits vitamin B6 biosynthesis to promote infection in rice. Plant Communications, 2022, 3(3): 100324. DOI:10.1016/j.xplc.2022.100324 |
 2023, Vol. 63
2023, Vol. 63